31.05.2022
18 мая 2022 года в журнале Journal of Clinical Oncology опубликованы результаты исследования 3 фазы EMERALD [1], посвященного изучению эффективности эласестранта в поздних линиях терапии гормонозависимого HER2-негативного рака молочной железы (РМЖ).
Работа вызывает большой клинический интерес, так как это первое успешное исследование 3 фазы, демонстрирующее эффективность нового перорального селективного деструктора эстрогеновых рецепторов (SERD). Ранее два SERD амсенестрант (Ameera-3, Sanofi) и гиредестрант (Acelera, Roche) не продемонстрировали эффективности в поздних линиях терапии гормонозависимого HER2-негативного РМЖ.
Активное внедрение в рутинную практику новых препаратов таргетной терапии (ингибиторов CDK4/6, mTOR, PI3K) при РЭ+/РП+ HER2-негативном РМЖ, назначающихся в комбинации с гормонотерапией, привело к острой нехватке именно гормональных партнеров. Большинство пациентов успевают получить гормонотерапию в адъювантных режимах или в первых линиях лечения, что делает затруднительным назначение эффективной комбинации, так как опции гормонотерапии исчерпаны. Еще одной проблемой является выявление у 20-40% пациенток, ранее получавших ингибиторы ароматазы, мутации в гене ESR1, приводящей к лиганд-независимой активации эстрогенового рецептора.
Эласестрант – селективный нестероидный пероральный деструктор эстрогеновых рецепторов (SERD) (рис.1). In vivo была продемонстрирована эффективность эласестранта на ксенотрансплантатных моделях, резистентных к ингибиторам CDK4/6, фулвестранту и с точечными мутациями в гене ESR1 (Y537S и D538G).
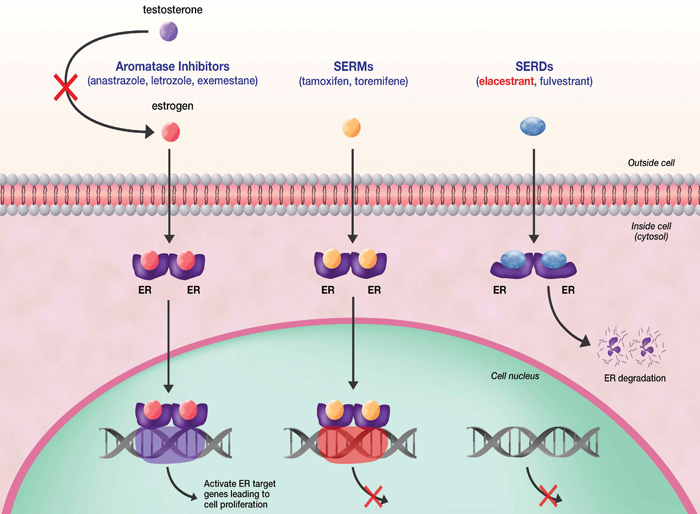
Рисунок 1. Механизм действия гормонотерапии при гормонозависимом HER2-негативном раке молочной железы.
В исследование EMERALD было включено 477 пациенток в менопаузе со статусом ECOG 0-1, в анамнезе у которых была 1 или 2 линии эндокринотерапии с включением ингибиторов CDK4/6 и/или 1 линия химотерапии по поводу диссеминированного или неоперабельного местнораспространенного гормонозависимого HER2-негативного РМЖ.
Пациентки были рандомизированы в 2 лечебные группы (1:1):
Стратификация в группы проводилась в зависимости от распространенности заболевания, статуса мутации ESR1 (Cuardant360 CDx) и предшествующей терапии.
Первичной конечной точкой исследования была медиана выживаемости без прогрессирования (ВБП) в группе пациенток с мутацией в гене ESR1, вторичными – медианы общей выживаемости (ОВ) и ВБП, частота объективного ответа, токсичность и переносимость терапии в общей группе больных.
Медиана возраста пациенток в исследовании достигла 63 лет (24-89), у 47,8% выявлена мутация в гене ESR1 и в 43,4% случаях в анамнезе 2 линии эндокринотерапии.
При медиане длительности наблюдения в 15,1 мес. медиана ВБП была значимо выше при назначении эласестранта в сравнении с терапией по выбору исследователя как в общей группе – 2,8 мес. против 1,9 мес. (ОР=0,77; 95% ДИ 0,55-0,88; p=0,002), так и при наличии мутации в гене ESR1 – 3,8 мес. и 1,9 мес. (ОР=0,55; 95% ДИ 0,39-0,77; p=0,0005) соответственно (рис.2, A и B).
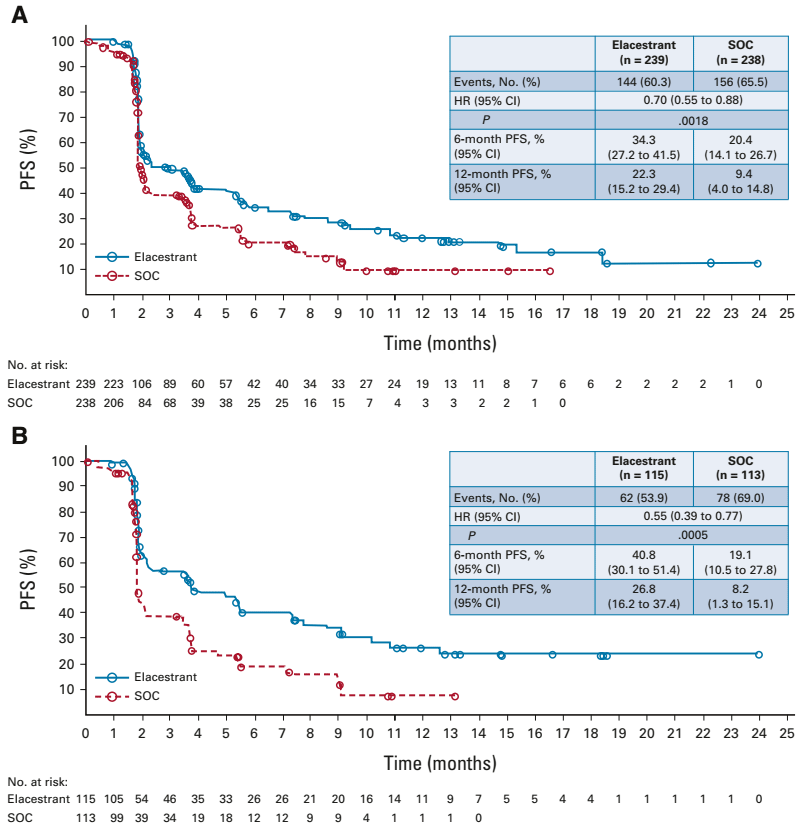
Рисунок 2.
A – выживаемость без прогрессирования в общей группе больных;
B – выживаемость без прогрессирования в группе пациентов с мутацией в гене ESR1.
Назначение эласестранта в сравнении со стандартной гормонотерапией позволило увеличить 12-месячную ВБП в общей когорте пациентов с 9,4% до 22,3% и в когорте пациентов с мутацией ESR1 с 8,2% до 26,8% соответственно.
При подгрупповом однофакторном анализе было показано, что эффективность эласестранта не зависит от распространенности заболевания (наличия висцеральных метастазов), статуса ECOG, количества линий эндокринотерапии и химиотерапии в анамнезе, при максимальном выигрыше у пациентов с мутацией в гене ESR1, старше 65 лет и ранее не получавших фулвестрант (рис.3).
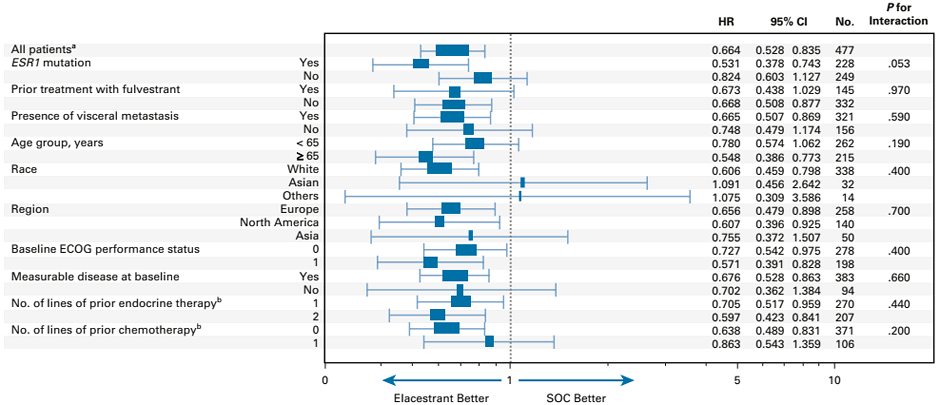
Рисунок 3. Однофакторный анализ.
Медианы ОВ в лечебных группах не достигнуты, при 12-месячной ОВ в группе с эласестрантом в 79,3% и 73,3% в группе стандартной терапии. В когорте пациентов с мутацией ESR1 12-месячная ОВ составила 82,6% и 73,6% соответственно.
Нежелательные явления (НЯ) в группах эласестранта и стандартной гормонотерапии преимущественно не превышали 1-2 степени и были представлены тошнотой (35,0% и 18,8%), слабостью (19,0% и 18,8%), рвотой (19,0% и 8,3%), снижением аппетита (14,8% и 9,2%) и болью в суставах (14,3% и 16,2%). НЯ 3-4 степени отмечены у 64 (27%) пациентов, получавших эласестрант, и у 47 (20,5%) в группе стандартной эндокринотерапии. В когорте эласестранта наблюдались НЯ 3-4 степени – тошнота (2,5%), боли в спине (2,5%) и повышение АЛТ (2,1%), а в когорте эндокринотерапии по выбору исследователя – тошнота (0,9%), слабость (0,9%) и диарея (0,9%); 15 и 10 пациентов соответственно прекратили терапию из-за неприемлемой токсичности.
Таким образом, эласестрант продемонстрировал эффективность в поздних линиях терапии гормонозависимого HER2-негативного рака молочной железы и приемлемый и управляемый профиль токсичности.
Источники: