27.10.2020

Совсем недавно описать первую линию химиотерапии (ХТ) при распространенном раке яичников (РЯ) можно было двумя предложениями. В первом постулате мы бы указали, что «золотым стандартом» первой линии неизменно являются 6 курсов ХТ паклитакселом и карбоплатином. Во втором, что в качестве поддерживающего лечения возможно добавление бевацизумаба у больных с неблагоприятным прогнозом течения заболевания (III-IV стадия с остаточными проявлениями после хирургического лечения). В настоящий момент ситуация кардинально изменилась, число возможных опций поддерживающего лечения увеличивается с каждым годом. Попытаемся разобраться в последних значимых исследованиях и новых показаниях.
Неоднократно жизнь показывает, что результат зависит от серьезности намерений и подходов. Так и при РЯ прогноз больной определяется не только характеристиками самой опухоли, но и качеством начального этапа лечения пациентки. Важным фактором является фактор хирурга, ответственно подходящего к своей задаче по выполнению максимальной циторедукции, четко оценивающего возможности первичного хирургического вмешательства на первом этапе и стремящегося к достижению этой цели. Химиотерапевты, которые занимаются лечением РЯ, отмечают, что в подавляющем большинстве пациентки распространенным РЯ достигают полного эффекта после первой линии ХТ и имеют максимально длительные сроки ремиссии именно после первой линии лечения. При этом отмечается хорошее качество жизни, позволяющее больным вернуться к обычному распорядку дня, почувствовать себя выздоровевшими и надеяться на излечение. Поэтому такое большое значение в лечении РЯ уделяется первой линии и поддерживающей терапии после нее. Задачей исследователей является максимально увеличить светлый промежуток до возникновения рецидива и перехода болезни в хроническое течение или, как конечная цель, излечить пациентку. Поэтому эксперты неоднократно просят уделять внимание именно этому этапу терапии РЯ, а именно адекватному и вовремя выполненному хирургическому вмешательству, соблюдению сроков начала ХТ первой линии, дозировок, графика введения цитостатических агентов и правильному назначению поддерживающего лечения.
В 2018 году изменился наш подход к лечению больных распространенным РЯ, когда появились первые данные исследования SOLO1 [1]. Результаты исследования SOLO1 позволили зарегистрировать олапариб в поддерживающем лечении после первой линии у больных III-IV стадий с патогенной мутацией BRCA1/2 в случае эффекта платиносодержащей терапии, в России это произошло в ноябре 2018 г. Исследование включало больных РЯ III-IV стадий с серозной High-Grade и эндометриоидной аденокарциномами (N=391) и наличием мутации в генах BRCA1/2. После проведения стандартной ХТ первой линии (паклитаксел и карбоплатин) и достижения полного или частичного эффекта пациентки рандомизировались на два рукава. В исследовательской группе больные получали олапариб в таблетированной форме 300 мг 2 раза в сутки в течение 2-х лет в качестве поддерживающего лечения, в контрольной группе – плацебо. Стоит напомнить, что когда результаты были доложены на ESMO 2018, то вся медицинская общественность, посвященная в проблему лечения РЯ, ликовала, поскольку появилась надежа на излечение такой категории больных или, как минимум, на достижение длительной ремиссии. Напомню, что за 3 года наблюдения медиана времени без прогрессирования (ВБП) не была достигнута в группе больных, получавших олапариб, в то время как в группе плацебо составила 13,8 мес. с момента рандомизации в исследование. Эти данные кардинально изменили нашу тактику: все пациентки РЯ III-IV стадий с серозным High-grade и эндометриоидным РЯ обязательно проходили тестирование на мутации в генах BRCA1/2 до начала или вовремя первой линии ХТ с целью идентификации больных с герминальными или соматическими мутациями в этих генах. Алгоритм определения мутации генов BRCA1/2 может включать в себя ПЦР диагностику для определения частых типичных герминальных мутаций, но при отрицательном результате обязательно требует полного геномного секвенирования (NGS) для исключения редких герминальных и соматических мутаций. Безусловно, онкологи столкнулись с трудностями тестирования, поскольку ПЦР-диагностика доступна в нашей стране, но проведение полного геномного секвенирования полностью ложится финансовым бременем на пациентку, а также является сложной методикой с биоинформатическим анализом, и не все лаборатории ею владеют полноценно. В настоящее время есть движение вперед, в ближайшем будущем часть регионов будет включать полногеномное секвенирование в программу ОМС.
Поданализ исследования SOLO1 продемонстрировал, что назначение олапариба становится предиктивным фактором, определяющим благоприятный прогноз течения заболевания у больных РЯ с мутацией генов BRCA1/2. У пациенток с интервальной циторедукцией, неоптимальным хирургическим вмешательством, получавших олапариб, в два-три раза увеличивается медиана ВБП по сравнению с группой плацебо. Важным является понимание специалистов, что назначение олапариба у таких больных не должно являться инструментом, прикрывающим погрешности наших хирургических возможностей. Поскольку выполнение полных оптимальных циторедукций на первом этапе с последующим назначением олапариба в поддержке позволяет превалирующему большинству больных иметь шанс на излечение.
Российские онкологи накопили за 2019-2020 годы собственный опыт лечения олапарибом больных РЯ с мутацией в генах BRCA1/2, в то же время с любопытством ожидая дальнейшего анализа исследования SOLO1. На ESMO 2020 были доложены результаты наблюдения за больными в течение 5 лет [2]. Важно отметить следующее. Во-первых, достигнута медиана ВБП в группе олапариба, она составила 56,0 мес., риск прогрессирования снижается на 67% (HR 0,33; 95% CI 0,25-0,43). Что это означает? Что в 50% случаев больные проживают более 4,5 лет без признаков прогрессирования! Это действительно революция в лечении распространенного РЯ, поскольку таких показателей не было получено до настоящего времени ни в одном исследовании. Ведь обычно медиана продолжительности жизни (ПЖ) таких больных составляет 49-56 мес., а здесь, еще раз подчеркиваю, это медиана ВБП! Во-вторых, частота возникновения прогрессирования не увеличивается после окончания приема олапариба через 2 года, и 48% больных переживает рубеж 5 лет без возврата болезни, тогда как в группе плацебо – только 21%, что соответствует данным литературы. В-третьих, для больных, достигших полного эффекта после ХТ первой линии, медиана ВБП не была достигнута после 5 лет наблюдения, 52% пациенток, получавших олапариб, не прогрессировали в течение этого времени, а в группе плацебо эта цифра составила 22% (HR 0,37; 95% CI 0,27-0,52). В-четвертых, такая же тенденция наблюдалась при оценке времени до последующего прогрессирования или смерти или времени до последующей терапии или наступления смерти. Таким образом, обновленные данные исследования SOLO1 безоговорочно подтверждают, что назначение олапариба в поддержке у больных распространенным РЯ с мутациями в генах BRCA1/2 позволяет надеяться на длительную ремиссию и даже на излечение.
Напомню, что в 2019 году эффективность поддерживающей терапии PARP ингибиторами была подтверждена публикацией данных нескольких исследований. В Европе и США зарегистрирован не только олапариб, но и нирапариб. В исследовании PRIMA пациентки с РЯ вне зависимости от мутации BRCA1/2 получали либо нирапариб, либо плацебо после окончания ХТ первой линии [3]. Результаты данного исследования позволили зарегистрировать поддерживающую терапию нирапарибом всем больным вне зависимости от статуса мутации BRCA1/2.
Встает логичный вопрос, где же теперь остается место бевацизумаба после 1-й линии химиотерапии? В 2019-2020 годах после регистрации олапариба в первой линии в России место бевацизумаба оставалось у больных распространенным РЯ III-IV стадий с наличием остаточной опухоли или неоперабельных вовсе, то есть больных с неблагоприятным прогнозом, при отсутствии у них мутации в генах BRCA1/2. В том случае, если бевацизумаб был начат совместно с первой линией терапии и у больной в процессе лечения выявлялась мутация BRCA1/2, рекомендовалось завершить терапию бевацизумабом и начать поддерживающую терапию олапарибом в течение двух лет, поскольку риск возникновения прогрессирования снижается в 3 раза при замене бевацизумаба на олапариб (таблица 1). И все было понятно, пока не были опубликованы результаты исследования PAOLA-1 [4].
Итак, перейдем подробно к этому неоднозначному исследованию. В работу было включено 806 пациенток с РЯ III-IV стадий, получивших хирургическое лечение и начавших ХТ 1-й линии. Пациентки начинали получать бевацизумаб во время ХТ. После окончания цитостатического лечения при достижении эффекта на терапию пациентки рандомизировались в два рукава. Контрольная группа получала стандартное лечение бевацизумабом в течение 15 мес. и плацебо. Экспериментальная группа – олапариб в таблетированной форме в течение 2 лет и бевацизумаб в течение 15 мес. Когда планировалось исследование, не было данных по подгрупповому анализу исследования ICON7, поэтому все пациентки в исследовании вне зависимости от группы прогноза получали стандартную химиотерапию и бевацизумаб в течение 15 мес. Первичной конечной точкой в исследовании была медиана ВБП. В обеих группах число больных с мутацией BRCA1/2 составило 30%. Хирургическая тактика больных, включенных в исследование, соответствует стандартам качественно работающего диспансера. В 50% случаев пациентки были прооперированы на первом этапе, при этом в большинстве случаев без остаточной опухоли (59% и 62%). В группе интервальных хирургических вмешательств цифра полных циторедукций достигала 71% и 68%. Получается, что согласно поданализу исследования ICON7, более половины больных не нуждались в добавлении бевацизумаба в поддерживающем режиме.
Перейдем к анализу результатов, доложенных на ESMO 2019. Медиана ВБП в группе комбинации олапариба и бевацизумаба составила 22,1 мес., в группе одного бевацизумаба – 16,6 мес. (HR=0,59; 95% CI 0,49-0,72; p<0,0001). Исследование позитивное, поскольку достигло первичной конечной точки. Однако исследователей интересовал вопрос, какая же группа получает наибольшую пользу от такой комбинации? По блокам больных, принимавших участие, был выполнен тест MYRIAD MyCHoice CD+. Это единственный одобренный FDA тест для выявления нарушений в системе гомологичной рекомбинации (HRD), который включает анализ только генов BRCA1/2, а именно мутации и оценки геномной нестабильности за счет крупных перестроек, потери гетерозиготности и алелльный дисбаланс теломеров в данных генах. Оценка проводится по бальной шкале. При наличии 42 баллов и более опухоль считается HRD позитивной, а при меньшем количестве баллов – HRD негативной. Уточню, что наличие патогенной мутации в генах BRCA1/2 априори является HRD+ опухолью. В исследовании PAOLA-1 практически половина больных оказались HRD позитивными (48%), т.е. 19% больных не имели патогенной мутации в генах BRCA1/2, но имели другие генетические изменения, приводящие к нарушениям в системе гомологичной репарации ДНК. У 34% больных (N=277) HRD статус был негативным, т.е. не определялась поломка в системе гомологичной репарации, а у 18% (N=142) эта характеристика была неизвестна. Далее авторы провели анализ у трех групп, в зависимости от HRD статуса: 1-я группа – это больные с мутацией в генах BRCA1/2 в опухоли; 2-я группа – это больные с HRD позитивным статусом при отсутствии мутации в генах BRCA1/2; 3-я группа – это пациентки с HRD негативными опухолями или неизвестным статусом. Начнем разбирать их по порядку.
Первая категория больных аналогична пациенткам в исследовании SOLO1, только число неоптимальных и интервальных операций в исследовании PAOLA несколько выше, поэтому сразу была достигнута медиана ВБП. Медиана ВБП в группе олапариба и бевацизумаба составила 37,2 мес., в группе только бевацизумаба – 17,7 мес., риск прогрессирования снижается на 67% при добавлении олапариба (HR 0,33, 95% CI 0,25-0,45). Другими словами, снижение риска прогрессирования в исследовании SOLO1, где пациентки получали один олапариб, и в исследовании PAOLA-1, где пациентки получали олапариб и бевацизумаб, одинаково (см. таблицу 1). В связи с этим международные эксперты пришли к выводу, что, не смотря на размер остаточной опухоли, группы прогноза, у пациенток с мутацией BRCA1/2 основную пользу несет олапариб, а добавление бевацизумаба не добавляет преимущества.
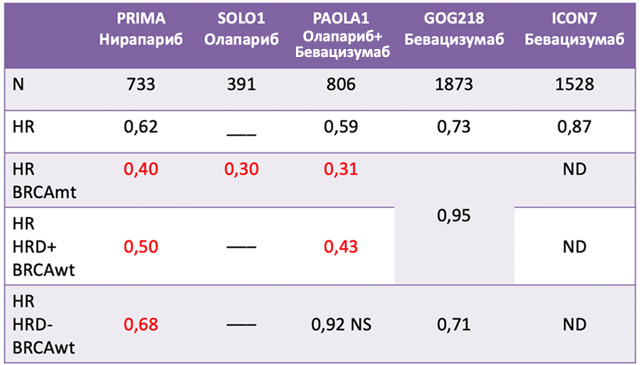
Таблица 1. Относительный риск прогрессирования у больных распространенным РЯ
в зависимости от вида поддерживающей терапии.
В группе HRD+ больных без мутации в генах BRCA1/2 также получено достоверное преимущество от использования комбинации. Медиана ВБП в группе олапариба и бевацизумаба составила 28,1 мес., в группе только бевацизумаба – 16,6 мес. (HR 0,43; 95% CI 0,28-0,66). В группе HRD негативных больных или в том случае, когда статус был неизвестен, не было получено достоверных преимуществ от добавления олапариба к бевацизумабу. Конечно, мы сожалеем, что в исследовании PAOLA не было третьего рукава, просто стандартного лечения, для того, чтобы понять, добавляет ли бевацизумаб достоверное преимущество, особенно в группе HRD позитивных больных.
На SGO 2020 был доложен поданализ в зависимости от времени и объема выполнения циторедукции [6]. Статистически значимое преимущество было показано только в группе больных без остаточной опухоли вне зависимости от времени выполнения циторедукции. В группе больных с резидуальной болезнью различия не были получены. Это может свидетельствовать в пользу добавления олапариба у больных с низким риском (полной циторедукцией), однако не свидетельствует о преимуществе добавления бевацизумаба.
На ESMO 2020 были проанализированы вторичные конечные точки, а именно ВБП2 (время без прогрессирования до последующего прогрессирования или смерти) [5]. Анализ более длительного наблюдения продемонстрировал сохранившуюся тенденцию. У больных с мутацией в генах BRCA1/2 медиана ВБП2 была достоверна выше в группе олапариба и бевацизумаба и преимущество составило 15 мес. (HR 0,56; 95% CI 0,41-0,77). В группе HRD позитивных больных без мутаций в генах BRCA1/2 польза от добавления комбинации равнялась 20,2 мес. по сравнению с одним бевацизумабом (HR 0,56; 95% CI 0,41-0,77). И наконец, в группе HRD негативных пациенток различия не были получены.
Перед тем как обсудить полученные результаты, обратимся к исследованию PRIMA, где статус HRD являлся фактором стратификации, а пациентки получали после первой линии ХТ только нирапариб или плацебо. Любопытно, что в этом исследовании во всех группах было получено достоверное преимущество от назначения поддерживающей терапии нирапарибом по сравнению с плацебо: максимальное преимущество – в группе больных с мутацией BRCA1/2, затем при наличии HRD+ статуса, а не столь значительное, но статистически достоверное – у больных с отсутствием HRD нарушений [3]. На основании этого исследования FDA и EMA зарегистрировали нирапариб в поддерживающем режиме после первой линии ХТ вне зависимости от BRCA и HRD статуса. Возникает логичный вопрос, если бы в данном исследовании к нирапарибу был добавлен бевацизумаб, отразилось бы это позитивно на результатах исследования? Или основной вклад в увеличение продолжительности ВБП вносят именно PARP ингибиторы, особенно у больных с мутацией BRCA1/2 и нарушениями в системе гомологичной рекомбинации?
Итак, в 2019 году в Европе и США зарегистрирована поддерживающая терапия нирапарибом у всех больных, поддерживающая терапия олапарибом у пациенток с наличием мутации в генах BRCA1/2, а в 2020 году регистрируется комбинация олапариба и бевацизумаба для больных с мутацией в генах BRCA1/2 и при наличии HRD+ опухоли. При обсуждении последнего показания международные эксперты сталкиваются с проблемой тестирования для выявления больных с нарушениями гомологичной рекомбинации. Сегодня существует только один тест компании Myriad Genetics для выявления популяции больных с нарушениями HRD. Стоимость этого теста Myriad myChoice CDx составляет 4040$, что является большой финансовой нагрузкой на систему здравоохранения Европы. Вероятно, стоимость теста снизится в следующем году, когда закончится патент на данное генетическое исследование у компании Myriad Genetics, что позволяет нам надеяться на доступность HRD тестирования в ближайшее время. Однако сегодня для наших пациентов проведение HRD тестирования является практически невозможным.
Россия не отстает от зарубежных коллег, Минздрав в 2020 году регистрирует комбинацию олапариба и бевацизумаба для всех больных раком яичников III-IV стадий вне зависимости от статуса BRCA и HRD после эффективной 1-й линии ХТ. Такое показание позволяет нам быть более свободными в выборе лечения, а с другой стороны, несет некоторую опасность. Во-первых, показание к назначению олапариба для всех больных снимает необходимость тестирования на выявление мутации BRCA1/2. А знание этого факта важно не только самим пациенткам и лечащим их онкологам, но и их родственникам. Поскольку позволяет выявлять здоровых носителей, осуществлять более пристальное наблюдение за ними и тем самым снизить частоту встречаемости наследственных онкологических заболеваний в стране. Во-вторых, первая линия лечения РЯ становится значительно дороже для нашей страны. К сожалению, реалии таковы, что мы не сможем обеспечить всех пациенток с распространенным РЯ данной комбинацией. При этом есть высокие риски, что больным с патогенными мутациями в генах BRCA1/2 может не достаться олапариба, а ведь это группа пациенток, которые могут быть излечены от данного заболевания. И наоборот, примерно 50% больных РЯ не имеют нарушений в системе гомологичной репарации и не будут получать пользы от олапариба с бевацизумабом, а будут иметь только побочные эффекты. В-третьих, использование этих двух дорогостоящих препаратов без селекции больных может ограничить возможность их использования у категории пациентов, где доказана эффективность каждого по отдельности. В-четвертых, решение о назначение комбинации должно быть принято ко времени начала первой линии химиотерапии, поскольку согласно инструкции мы не можем назначить комбинацию олапариба и бевацизумаба после окончания первой линии терапии, поскольку в исследовании все пациенты получали бевацизумаб вместе с ХТ.
В то же время положительным моментом данной регистрации является мотивация ученых и генетиков на острую необходимость разработки собственного теста для выявления нарушений в системе гомологичной репарации (HRD). Этим как раз сейчас занимаются молекулярные генетики, а также компания AstraZeneca, которая уже имеет опыт по внедрению BRCA1/2 тестирования в нашей стране.
Экспертное сообщество обращает ваше внимание на сознательный и вдумчивый подход к назначению комбинации олапариба и бевацизумаба в поддержке после первой линии терапии у больных без мутации BRCA1/2. В таблице 2 представлен возможный алгоритм. Призываем стараться определять мутацию в генах BRCA1/2 на самом раннем этапе, поскольку в случае наличия мутации в поддерживающем режиме обязательно рекомендовано назначение PARP ингибитора. Если вы не удержались и назначили бевацизумаб вместе с первой линией, то ориентируйтесь на статус мутации BRCA1/2, какой ответ достигнут на проведенную ХТ. Также помним, что в условиях нашей реальности назначение бевацизумаба максимально эффективно у больных с остаточными признаками болезни после операции, у неоперабельных больных, то есть в тех ситуациях, когда опухоль является агрессивной, а заболевание выявляется при значительном распространении болезни.
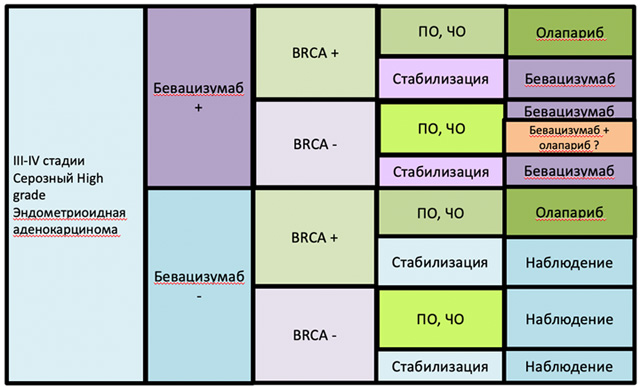
Таблица 2. Возможный алгоритм выбора поддерживающей терапии у больных распространенным РЯ.
В заключение хочется отметить, что c каждым годом у нас появляются новые опции в лечении распространенного РЯ, современные лабораторные тесты, что позволяет нам внедрять новейшие возможности и видеть перспективы научного продвижения вперед. Сегодня при правильном комплексном подходе хирургов, химиотерапевтов и адекватном лекарственном лечении мы можем позволить себе сказать пациентке с распространенным РЯ, что у нее есть шанс на излечение.
Список литературы: