01.10.2020
 Семиглазова Татьяна Юрьевна
Семиглазова Татьяна Юрьевна Шарашенидзе Софико Мамуковна
Шарашенидзе Софико МамуковнаC 19 по 21 сентября 2020 года состоялся виртуальный конгресс Европейского общества клинической онкологии (ESMO). Конгресс ESMO2020 объединил более 30 тыс. специалистов из 150 стран мира, представивших 2137 абстрактов. Категория late-breaking abstract (LBA) была присвоена 87 научным тезисам. Более 15 докладов были посвящены актуальным вопросам лечения больных раком молочной железы (РМЖ). В данном обзоре представлены результаты ряда исследований по системному лечению пациентов с метастатическим и ранним РМЖ, представленных на Конгрессе ESMO2020.
Конгресс ESMO2020 еще раз подтвердил, что современная концепция системного лечения больных РМЖ – это комбинированная терапия с учетом биологического подтипа опухоли и таких важных мишеней, как рецепторы эстрогенов, экспрессия HER2, PD-L1-экспрессия, мутация PIK3CA и мутация gBRCA1/2. При этом важно помнить, что мы лечим не рак, а больного со злокачественной опухолью, основываясь на пациент-центрированном, проблемно-ориентированном, максимально индивидуализированном подходе с учетом всей доказательной базы о биологии опухоли и ее реакции на системное лечение.
МЕТАСТАТИЧЕСКИЙ РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
Трижды негативный метастатический РМЖ
Miles и соавт. представили результаты исследования IMPASSION131 по изучению эффективности комбинации атезолизумаб+паклитаксел vs паклитаксел+плацебо в 1-й линии терапии больных нерезектабельным местнораспространенным или метастатическим трижды негативным РМЖ (мТНРМЖ) [1].
Отрицательный результат исследования IMPASSION131 – это тоже результат.
Исследователи не получили статистически значимого увеличения ВБП (рис.1) ни у больных PD-L1+ мТНРМЖ (медиана ВБП составила 6,0 мес. в группе больных атезолизумаб+паклитаксел vs 5,7 мес. в группе плацебо+паклитаксел (ОР=0,82; 95% ДИ 0,60-1,12; р=0,20)), ни в общей популяции больных (5,7 мес. и 5,6 мес. соответственно; ОР=0,86; 95% ДИ 0,70-1,05).
Результаты по вторичной точке исследования общей выживаемости (ОВ) – также негативные. В группе больных PD-L1+ мТНРМЖ медиана ОВ составила 28,3 мес. в группе плацебо+паклитаксел vs 22,1 мес. атезолизумаб+паклитаксел соответственно (ОР=1,55; 95% ДИ 0,86-2,80), в общей группе ОВ – 22,8 мес. в группе плацебо+паклитаксел vs 19,2 мес. атезолизумаб+паклитаксел соответственно (ОР=1,31; 95% ДИ 0,94-1,82).
Авторами отмечено, что одной из возможных причин неудачи данного исследования по сравнению с исследованием IMPASSION130, помимо различий химиотерапевтических режимов, являлась необходимость назначения дексаметазона в качестве премедикации к паклитакселу (в отличие от наб-паклитаксела), которое в свою очередь могло снижать эффективность атезолизумаба.
Несмотря на негативный результат, авторы признают значимость исследования в очередном доказательстве необходимости понимания взаимодействия опухоли и иммунной системы, а также роли выбора комбинаторного химиотерапевтического партнера к иммунотерапии.
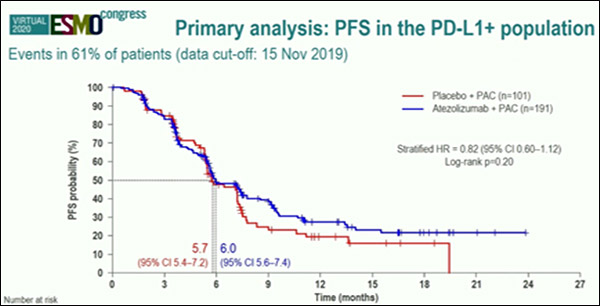
Рисунок 1. Исследование III фазы IMPASSION131: эффективность 1-й линии терапии
атезолизумаб+паклитаксел vs паклитаксел+плацебо у больных PDL+ мТНРМЖ.
Напротив, исследование IMPASSION130 (Emens и соавт.), в котором медиана наблюдения составила 18,8 мес. (8,9-34,7 мес.), продемонстрировало преимущество в ОВ (рис.2) при лечении больных PD-L1+ мТНРМЖ атезолизумаб+наб-паклитаксел vs плацебо+наб-паклитаксел:
Тогда как в общей группе пациентов (независимо от статуса PD-L1) статистически значимая граница ОВ не была достигнута (ОР=0,87; 95% ДИ 0,75-1,02; p=0,077), что исключает дальнейшее изучение комбинации атезолизумаб+наб-паклитаксел в данной популяции пациентов.
Наиболее частыми нежелательными явлениями в группе атезолизумаб+наб-паклитаксел были кожная сыпь, гипотиреодизм и гипертиреодизм. Нежелательные явления 3-4 степени наблюдались у 51% пациентов в группе атезолизумаб+наб-паклитаксел vs 43% в группе плацебо+наб-паклитаксел. Отмена терапии (наиболее часто по причине нейропатии) потребовалась в 19% случаев в группе атезолизумаб+наб-паклитаксел vs 8% в группе плацебо+наб-паклитаксел.
Таким образом, более зрелые позитивные результаты исследования IMPASSION130 подтвердили преимущество назначения анти-PDL-ингибиторов в комбинированной терапии атезолизумаб+наб-паклитаксел 1 линии системной терапии PD-L1+ мТНРМЖ.
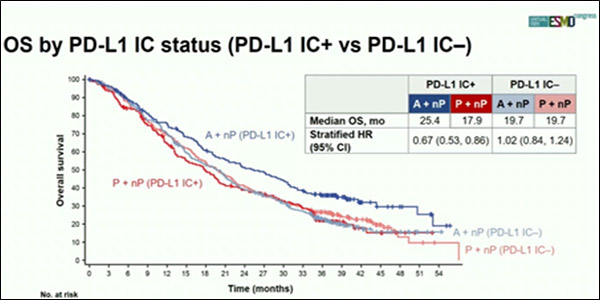
Рисунок 2. Исследование III фазы IMPASSION130: эффективность 1-й линии терапии
атезолизумаб+наб-паклитаксел vs наб-паклитаксел+плацебо у больных PD-L1+ мТНРМЖ.
В ходе конгресса были доложены результаты позитивного исследования ASCENT (Bardia и соавт.) по изучению применения сацитизумаба говитекана vs терапия по выбору врача (ТВВ) среди пациентов, уже получавших не менее 2-х линий терапии по поводу мТНРМЖ [3].
Сацитизумаб говитекан – конъюгат моноклонального антитела к TROP2 плюс активный метаболит химиотерапевтического препарата иринотекана. Для справки: TROP2 – это опухоль-ассоциированный трансдуктор кальциевого сигнала-2, который экспрессируется при всех подтипах РМЖ. В апреле 2020 года FDA одобрило сацитузумаб говитекан для лечения больных мТНРМЖ, получавших 2 и более линии терапии.
В исследовании ASCENT проанализированы сведения о 468 больных мТНРМЖ (медиана возраста 54 года, в анамнезе в среднем 4 линии предшествующей системной терапии). Исследователями отмечено несомненное преимущество как в ВБП (5,6 мес. в группе сацитизумаба говитекана vs 1,7 мес. в группе ТВВ; ОР=0,41; р<0,0001), так и в ОВ (рис.3) (12,1 vs 6,7 мес. соответственно; ОР=0,48; р<0,0001). Частота объективного ответа составила 35% в группе сацитузумаба говитекана vs 5% в группе ТВВ (р<0,0001).
Исследование подверглось некоторой критике в связи с выбором конечной точки: при мТНРМЖ, особенно после 2 линии терапии, первичной конечной точкой следует выбирать ОВ, а не ВБП.
Сацитузумаб говитекан удовлетворительно переносится, характеризуется управляемым профилем безопасности. Основными нежелательными явлениями были гематологическая токсичность, желудочно-кишечная токсичность (тошнота, диарея) и астения. Осложнениями (степень ≥3), связанными с сацитузумабом говитеканом (n=258) vs ТВВ (n=224), были нейтропения (51% vs 33%), диарея (10,5% vs <1%), анемия (8% vs 5%) и фебрильная нейтропения (6% vs 2%). В данном исследовании не были зарегистрированы серьезная кардиотоксичность; нейропатия >3 степени; интерстициальное поражение легких и смерть, ассоциированная с лечением сацитузумабом говитеканом.
Таким образом, иммуноконъюгат сацитузумаб говитекан становится новым стандартом системной терапии предлеченных пациентов с трижды негативным метастатическим РМЖ.
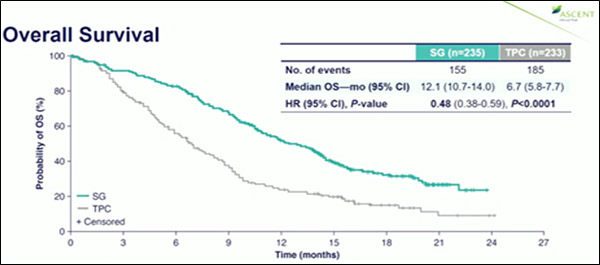
Рисунок 3. Исследование III фазы ASCENT: эффективность терапии говитекан сацитузумаб
vs химиотерапия у больных мТНРМЖ, получавших 2 и более линий терапии.
В этом году на ESMO были доложены обнадеживающие результаты исследования SOLAR-1 по общей выживаемости у больных ER+ HER2- мРМЖ с мутацией в гене PIK3CA, получавших комбинацию алпелисиб+фулвестрант vs плацебо+фулвестрант [4].
Мутация гена PIK3CA – маркер неблагоприятного прогноза, который обнаруживается уже на ранних стадиях в первичной опухоли и сохраняется в очагах метастазирования на более поздних стадиях. Нарушения в PI3K-зависимом каскаде характерны для всех типов РМЖ. Приблизительно у 40% пациентов с ER+ HER2- мРМЖ может быть обнаружен мутантный ген PIK3CA, приводящий к гиперактивации PI3K-Akt-mTOR сигнального каскада. Это в свою очередь приводит к эстроген-независимой стимуляции ER+ РМЖ и, как следствие, резистентности к гормонотерапии.
Алпелисиб – селективный ингибитор каталитической субъединицы αPI3K. Ранее сообщалось о статистически значимом улучшении ВБП среди пациентов PIK3CAm+ ER+ HER2- мРМЖ (11,0 мес. в группе алпелисиб+фулвестрант vs 5,7 мес. в группе плацебо+фулвестрант; ОР=0,65; 95% ДИ 0,50-0,85; p=0,00065).
Согласно представленным на Конгрессе результатам André и соавт., выигрыш в ОВ (рис.4) составил 7,9 мес. (39,3 мес. и 31,4 мес. соответственно; ОР=0,86; 95% ДИ 0,64-1,15; p=0,15). Однако показатели ОВ в окончательном анализе не пересекли заранее оговоренную границу эффективности O’Brian Flemming (p≤0,0161).
Среди пациентов с PIK3CAm+ ER+ HER2- мРМЖ с метастазами в печени и/или легких медиана ОВ в группе алпелисиб+фулвестрант достигла 37,2 мес. (95% ДИ 28,7-43,6) vs 22,8 мес. (95% ДИ 19,0-26,8) в группе плацебо+фулвестрант (ОР=0,68; 95% ДИ 0,46-1,00). Также было отмечено увеличение во времени до применения первой химиотерапии в группе алпелисиб+фулвестрант до 8,5 мес. (ОР=0,72; 95% ДИ 0,54-0,95).
Основными и ожидаемыми побочными эффектами комбинации алпелисиб+фулвестрант были гипергликемия (64,8%), диарея (59,5%), тошнота (46,8%), рвота (28,5%) и кожная сыпь (36,3%). Редукция доз алпелисиба наблюдалась в 74% случаев.
Поскольку гипергликемия является «таргетным» осложнением, то и при назначении алпелисиба необходимо принимать во внимание наличие у пациентов сопутствующих заболеваний, в особенности сахарного диабета и уровень исходного HbA1c.
Примечание: Гипергликемия на фоне приема алпелисиба ≠ сахарный диабет.
С учетом ранее полученного статистически значимого увеличения ВБП, результатов общей выживаемости (несмотря на отсутствие статистической значимости, добавление алпелисиба к фулвестранту увеличивает ОВ на 7,9 месяца), крайне актуально применение комбинации алпелисиб+фулвестрант в группе пациентов неблагоприятного прогноза с PIK3CA-мутированным ЕR+ HER2- мРМЖ.
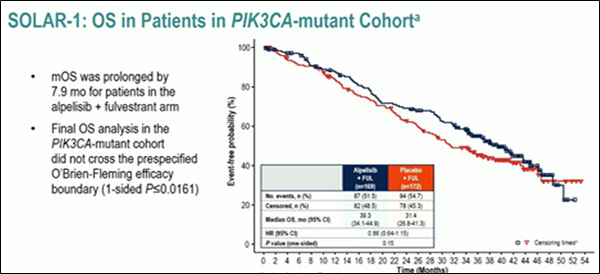
Рисунок 4. Исследование III фазы SOLAR-1: эффективность 2-й линии терапии алпелисиб+фулвестрант
vs фулвестрант+плацебо у больных PIK3CAm+ ЕR+ HER2-мРМЖ, получавших ингибиторы ароматазы.
ER+HER2- метастатический РМЖ
В ходе конгресса были озвучены результаты окончательного анализа 2-летней общей выживаемости исследования II фазы nextMONARCH (Hamilton и соавт.) при применении монотерапии абемациклибом или комбинации абемациклиба с тамоксифеном у пациентов с ER+HER2- мРМЖ [5]. Пациенты были рандомизированы в 3 группы: абемациклиб 150 мг + тамоксифен, абемациклиб 150 мг или абемациклиб 200 мг + профилактический прием лоперамида. При первичном анализе ВБП добавление тамоксифена продемонстрировало преимущество, однако незначимое статистически (9,1 мес. и 7,4 мес. соответственно; ОР=0,815; р=0,293). Выигрыш в ОВ (рис.5) составил 7,2 мес. при добавлении тамоксифена к абемациклибу, 24,2 мес. vs 17,0 мес. в группе монотерапии абемациклибом (ОР=0,62; 95% ДИ 0,40-0,97; p=0,0341). Медиана ОВ при монотерапии абемациклибом 150 мг составила 20,8 мес. и была сравнима с монотерапией абемациклибом в большей дозе 200 мг (ОР=0,96; 95% ДИ 0,64-1,44; p=0,8321). Диарея и гематологическая токсичность регистрировались реже в исследовании nextMONARCH по сравнению с исследованием MONARCH1: частота осложнений 3 степени составила 9% по сравнению с 20% соответственно.
Таким образом, добавление абемациклиба к тамоксифену обеспечило статистически значимое улучшение ОВ среди популяции предлеченных пациентов ER+HER2- мРМЖ.
Примечание: До представления данных результатов была полная уверенность, что гормонотерапия тамоксифеном станет уделом исключительно адъювантной терапии. Исследование nextMONARCH доказало, что тамоксифен может быть комбинаторным партнером к абемациклибу без риска нарастания токсичности.
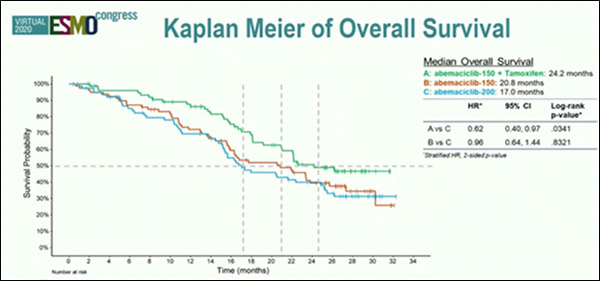
Рисунок 5. Исследование II фазы nextMONARCH: эффективность терапии абемациклиб в дозировке 150 мг + тамоксифен vs абемациклиб в дозировке 150 мг vs абемациклиб в дозировке 200 мг + профилактический прием лоперамида у больных HR+ HER2- РМЖ, получавших гормонотерапию и химиотерапию.
Albanell и соавт. представили позитивные результаты II фазы исследования FLIPPER: фулвестрант+палбоциклиб vs фулвестрант+плацебо в 1-й линии лечения ER+ HER2- мРМЖ [6]. Согласно результатам исследования, в группе комбинированной терапии фулвестрант+палбоциклиб было достигнуто статистически значимое улучшение 1-годичной ВБП (рис.6) (83,5% vs 71,9% соответственно; ОР=0,55; 80% ДИ 0,36-0,83; p=0,064). Также было отмечено улучшение медианы ВБП и частоты объективного ответа. Данные об ОВ на данный момент предварительные.
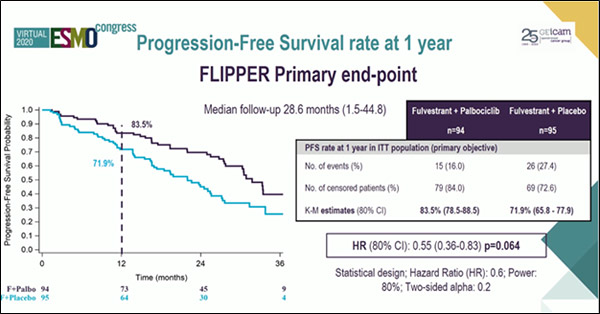
Рисунок 6. Исследование II фазы FLIPPER: эффективность 1-й линии терапии
фулвестрант+палбоциклиб vs фулвестрант+плацебо у больных HR+ HER2- метастатическим РМЖ.
РАННИЙ РМЖ
ER+ HER2- ранний РМЖ
В ходе Конгресса (исследование MONARCHE) были доложены своего рода революционные результаты – добавление таргетного препарата CDK4/6 ингибитора абемациклиба к адъювантной эндокринотерапии у пациентов с ER+ HER2- ранним РМЖ группы высокого риска достоверно увеличивает безрецидивную выживаемость.
В исследование были включены сведения о 5637 больных ER+ HER2- ранним РМЖ группы высокого риска, которые рандомизировались 1:1 в группу комбинированной терапии абемациклиб (150 мг дважды в день 2 года) + стандартная адъювантная гормонотерапия vs стандартная адъювантная гормонотерапия (АГТ). Средний возраст больных в исследовании MONARCHE составил 51 год (12,6% пациентов в возрасте 40 лет), в основном женщины (99,4%) и в постменопаузе на время постановки диагноза (56,5%). У 60% были зарегистрированы региональные метастазы в 4-х и более лимфатических узлах. Адъювантную лучевую терапию получили 95,4%; химиотерапию – 95,4% больных (37% – НАХТ; 58,3% – АХТ; 3,5% – оба варианта). Адъювантную гормонотерапию (АГТ) ингибиторами ароматазы (ИА) получили 68,3% больных (включая 14,2% ИА плюс супрессия овариальной функции) и АГТ тамоксифеном – 31,4% (включая 7,6% тамоксифен плюс супрессия овариальной функции).
Медиана наблюдения в исследовании составила 15,5 мес. Добавление абемациклиба к адъювантной эндокринотерапии у пациентов с ER+ HER2- рРМЖ группы высокого риска на 25,3% (статистически значимо) увеличило безрецидивную выживаемость (рис.7) (ОР=0,75; 95% ДИ 0,60-0,93; p=0,01) – если быть точнее, то выживаемость без инвазивного РМЖ (Invasive disease-free survival, IDFS). Двухлетняя IDFS составила 92,2% и 88,7% соответственно.
Также на комбинированной таргетной терапии у пациентов были значимо выше показатели выживаемости без отдаленных метастазов (Distant relapse-free survival, DRFS) (ОР=0,72; 95% ДИ 0,56-0,92; p=0,01). Двухлетняя DRFS составила 93,6% в группе абемациклиба и 90,3% в контрольной группе. Отдаленные метастазы были зарегистрированы у 106 больных в группе комбинированной терапии абемациклиб+АГТ vs у 152 больных в группе АГТ. Общими локализациями отдаленных метастазов были кости (у 32 больных в группе абемациклиб+АГТ vs у 81 больных в группе АГТ), печень (29 vs 42), легкие (21 vs 21) и церебральные метастазы (17 vs 18).
В группе абемациклиба наиболее частыми побочными эффектами были диарея, нейтропения, усталость, тогда как в контрольной группе – артралгии, приливы, усталость. Нейтропения 3 степени была зарегистрирована у 20% больных на абемациклибе; фебрильная нейтропения отмечена у 0,3% больных. Диарея развивалась в среднем на 8 день, была непродолжительной (медиана длительности диареи 2 и 3 степени составляла от 5 до 6 дней). Контролировалась диарея успешно противодиарейными препаратами и коррекцией дозы. Частота диареи 3 степени составила 7,6%, однако только 4,8% больных прекратили терапию абемациклибом по причине диареи.
Таким образом, абемациклиб является первым CDK4/6 ингибитором, который при добавлении к стандартной адъювантной гормонотерапии продемонстрировал статистически значимое улучшение безрецидивной выживаемости у пациентов с ER+ HER2- ранним РМЖ группы высокого риска [7].
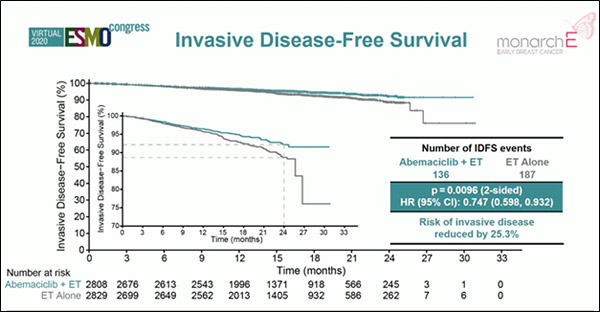
Рисунок 7. Исследование III фазы MОNARCHE: эффективность адъювантной терапии
абемациклиб+гормонотерапия vs гормонотерапия у больных HR+ HER2- ранним РМЖ группы высокого риска.
Напротив, исследование PALLAS (Mayer и соавт.), сравнивавшее адъювантную терапию палбоциклиб+АГТ vs стандартная АГТ у пациентов с ER+ HER2- РМЖ с II-III стадиями следует считать негативным. Исследователям не удалось доказать преимущество в БРВ (рис.8) (88,2% и 88,5% соответственно; ОР=0,93; 95% ДИ 0,76-1,15; p=0,51) [8]. Подгрупповой анализ также не выявил категорию пациентов, получающих преимущество от добавления к гормонотерапии палбоциклиба, включая пациентов с высоким риском рецидива. Негативный результат вероятно объясняется включением в исследование преимущественно больных ER+HER2- рРМЖ группы неблагоприятного прогноза: 60% относились к группе высокого риска и 80% пациентов проводилась адъювантная химиотерапия. Поэтому с целью понимания особенностей механизма действия CDK4/6 ингибиторов в лечении больных ER+ HER2- ранним РМЖ в настоящий момент инициирована трансляционная клиническая программа TRANSPALLAS.
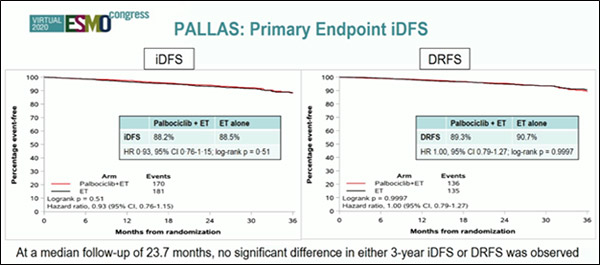
Рисунок 8. Исследование III фазы PALLAS: эффективность адъювантной терапии
палбоциклиб+гормонотерапия vs гормонотерапия у больных HR+HER2- ранним РМЖ.
Трижды негативный ранний РМЖ
В успешном исследовании IMPASSION031 (Harbeck и соавт.) среди пациентов с рТНРМЖ были изучены эффективность и безопасность атезолизумаба в сочетании с неоадъювантной химиотерапией (наб-паклитаксел или доксорубицин+циклофосфамид) [9]. В общей группе больных добавление атезолизумаба к НАХТ статистически значимо увеличивало частоту полных регрессов (рис.9) (pCR; ypT0/isN0) до 57,6% vs 41,1% в группе плацебо+НАХТ (р=0,0044).
Среди PD-L1+ популяции пациентов частота полных патоморфологических регрессов (pCR; ypT0/isN0) составила 68,8% в группе атезолизумаб+НАХТ и 49,3% в группе плацебо+НАХТ, что не являлось статистически значимым (р=0,021), так как граница статистической значимости была заявлена как р=0,0184. Медиана ВБП не была достигнута в обеих группах (ОР=0,76; 95% ДИ 0,40-1,44).
Наиболее частые нежелательные явления были схожи в группах и в основном были ассоциированы с химиотерапией.
По предварительным данным, в группе атезолизумаб+НАХТ было отмечено увеличение БРВ и ОВ. Важно, что среди пациентов с ранним ТНРМЖ применение комбинации атезолизумаба с НАХТ значимо увеличивает частоту полных патоморфологических регрессов независимо от PD-L1 статуса.
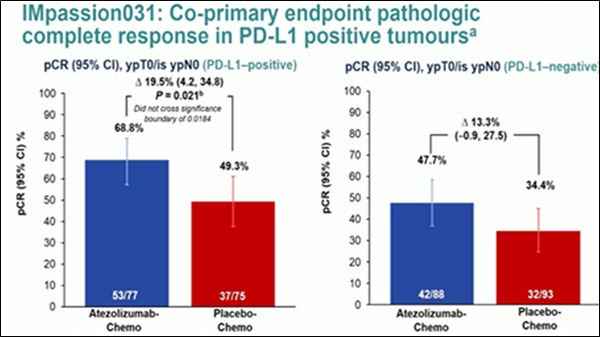
Рисунок 9. Исследование III фазы IMpassion031: эффективность неоадъювантной терапии
атезолизумаб+наб-паклитаксел vs наб-паклитаксел+плацебо у больных ранним ТНРМЖ.
De Jong и соавт. были доложены сведения о прогностической значимости TILs (опухоль-инфильтрирующих лимфоцитов) у молодых пациентов с ранним ТНРМЖ, не получавших адъювантную терапию [10]. Пациенты с высоким уровнем опухоль-инфильтрирующих лимфоцитов (более 75%) без (нео-)адъювантной терапии имели лучший прогноз (рис.10), ОВ в течение 15 лет достигала 93%. В то время как среди пациентов с низким уровнем TILs общая выживаемость в течение 15 лет составила 59%. Однако частота возникновения вторых опухолей в течение 15 лет была несколько выше в группе пациентов с высоким уровнем TILs (23 vs 14%).
Таким образом, уровень опухоль-инфильтрирующих лимфоцитов (TILs) исследователями рассматривается в качестве потенциального прогностического биомаркера в исследованиях по изучению деэскалации химиотерапии у больных ранним РМЖ.
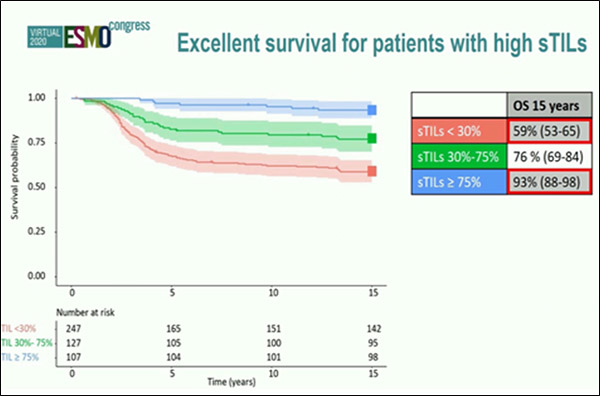
Рисунок 10. Прогностическая значимость опухоль-инфильтрирующих лимфоцитов
среди молодых пациентов ранним ТНРМЖ, не получивших (нео-)адъювантную системную терапию.
Schneeweiss и соавт. представили результаты исследования GEPAROCTO, сравнивающего у больных ранним РМЖ группы высокого риска НАХТ дозоинтенсивным режимом iddEPC (3 цикла эпирубицина каждые 2 недели + 3 цикла паклитаксела каждые 2 недели + 3 цикла циклофосфамида каждые 2 недели) vs PM(Cb) (еженедельный паклитаксел + липосомальный доксорубицин ± карбоплатин у больных ТНРМЖ) [11]. Больные HER2+ РМЖ также получали двойную анти-HER2 блокаду каждые 3 недели совместно с паклитакселом и циклофосфамидом. Медиана наблюдения составила 47,0 (1,6-61,5) месяцев.
Первичной конечной точкой исследования являлась частота pCR, которая статистически значимо не различалась в исследуемых группах дозоинтенсивного режима iddEPC и еженедельного режима PM(Cb) (48,3% vs 48,0%; ОР=0,99; 95% ДИ 0,77-1,28; p=0,979). Не было отмечено статистически значимого различия БРВ (ОР=1,16; 95% ДИ 0,85-1,59; p=0,3357) и ОВ (ОР=1,16; 95% ДИ 0,85-1,59; p=0,3357) соответственно. Однако среди пациентов с высоким уровнем TILs было отмечено преимущество в частоте pCR при дозоинтенсивном режиме.
У больных HER2+ РМЖ или ТНРМЖ различий в выживаемости на фоне проводимой НАХТ зарегистрировано не было.
В то же время у больных ER+ HER2- РМЖ на дозоинтенсивном режиме iddEPC отмечалось увеличение БРВ и ОВ. В группе PM(Cb) БРВ составила 62,5% vs 77,9% в группе iddEPC (ОР=2,11; 95% ДИ 1,08-4,10; p=0,0284); 4-летняя ОВ – 80,1% vs 94,7% соответственно (ОР=3,26; 95% ДИ 1,06-10,00; p=0,0388), но без корреляции с увеличением частоты pCR. Докладчиком был отмечен возможный иммуногенный долгосрочный эффект циклофосфамида при лечении больных ER+ HER2- рРМЖ группы высокого риска.
Продолжение Конгресса ESMO следует 16-18 октября 2020.
Источники: