08.06.2020

Немелкоклеточный рак легкого (НМРЛ) характеризуется ранним метастазированием после радикальных оперативных вмешательств: 5-летняя безрецидивная выживаемость составляет для IB стадии – 55%, для II – 38% и 24% для III [1]. Это свидетельствует о необходимости проведения системной адъювантной терапии. Современная адъювантная химиотерапия платиновыми дуплетами обладает низкой эффективностью, увеличивая 5-летнюю общую выживаемость лишь на 5%. Это не вызывает удивления, зная более чем скромные результаты химиотерапии при лечении НМРЛ на стадии метастатического процесса.
Прошло почти 15 лет после того, как была отмечена высокая результативность ингибиторов тирозинкиназы у больных метастатическим НМРЛ с наличием активирующей мутации гена EGFR. Три поколения препаратов этой группы стали стандартной первой линией системной терапии, увеличив продолжительность жизни с 8-10 месяцев до 24-36 месяцев. Результаты назначения ингибиторов тирозинкиназы в качестве адъювантной терапии у больных НМРЛ с наличием активирующей мутацией гена были не столь оптимистичны. В исследовании II фазы SELECT, изучавшем назначение ингибитора первого поколения эрлотиниба, и в исследовании ADJUVANT, сравнивающем адъювантное назначение гефитиниба с химиотерапией цисплатином и винорелбином, были получены убедительные свидетельства об увеличении медианы времени до прогрессирования [2, 3]. В обоих исследованиях длительность приема препаратов составляла 2 года. В исследовании SELECT 2- и 5-летняя безрецидивная выживаемость составила 88% и 56%, 5-летняя общая выживаемость – 56%, что существенно лучше исторических данных. Однако это исследование было нерандомизированным, включало большое количество больных IA стадии и скорее демонстрирует перспективность назначения ингибиторов тирозинкиназы, чем их реальную пользу. В исследовании ADJUVANT, несмотря на существенное увеличение продолжительности медианы времени до прогрессирования, при более длительном наблюдении отмечалось существенное увеличение частоты прогрессирования после отмены приема гефитиниба, и разница в 3-летней безрецидивной выживаемости составила всего 7% (34% в группе гефитиниба и 26% в группе химиотерапии). Эти результаты скорее свидетельствуют о способности гефитиниба отодвигать по времени развитие рецидива, чем о его способности достигать излечения. Эти неубедительные данные не позволяли рекомендовать ингибиторы тирозинкиназы первых поколений в качестве адъювантной терапии операбельных больных НМРЛ.
Осимертиниб является представителем третьего поколения ингибиторов тирозинкиназы, способным блокировать активность EGFR как в случае появления активирующей мутации в 19 и 21 экзонах, так и при возникновении мутации резистентности к ингибиторам первого второго поколения – T790M. В исследовании FLAURA осимертиниб у больных с метастатическим процессом продемонстрировал достоверный выигрыш в увеличении медианы времени до прогрессирования и общей выживаемости в сравнении с назначением гефитиниба или эрлотиниба. В связи с этим логичным выглядит изучение эффективности осимертиниба в качестве адъювантной терапии у больных операбельным НМРЛ.
ADAURA – это рандомизированное двойное-слепое исследование, в котором сравнивали эффективность осимертиниба и наблюдения за больными НМРЛ [4]. Включались больные IB-IIIА стадиями НМРЛ с активирующими мутациями (ex19del или L858R) после радикальной операции и окончания адъювантной химиотерапии, если она проводилась. Интервал между выполнением операции и включением в протокол не должен был превышать 10 недель для больных без адъювантной терапии и не более 26 недель от момента окончания адъювантной терапии. Рандомизация проводилась с учетом стратификационных факторов: стадия (IA vs II vs IIIA), мутация (ex19del vs L858R) и раса (европеоидная vs азиатская). Больные в группе осимертиниба принимали препарат в дозе 80 мг внутрь ежедневно в течение 3 лет. Первичной конечной точкой была безрецидивная выживаемость в группе больных II-IIIA стадий, вторичными были безрецидивная и общая выживаемость для всех включенных больных, токсичность и качество жизни.
Исследование было расслеплено решением независимого комитета, мониторирующего исследование, в связи с высокой эффективностью в группе осимертиниба. На момент расслепления все запланированные больные были включены в исследование и прослежены не менее 1 года от момента рандомизации.
В исследование было включено 682 больных медианой возраста 63 года, преимущественно женщины (70%), азиаты (64%), с распределением по стадиям: IB – 31%, II – 34%, IIIA – 35%, из которых 56% получали адъювантную химиотерапию с включением цисплатина. Медиана времени до прогрессирования больных II-IIIA стадий составила 20,4 мес. в группе наблюдения и не достигнута в группе осимертиниба, 3-летняя безрецидивная выживаемость составила 28% и 80%, что соответствует достоверному снижению относительного риска прогрессирования на 83% (HR=0,17; p<0,0001). Показатель 3-летней безрецидивной выживаемости (рис. 1) для всех больных составил 79% и 41% соответственно со снижением относительного риска прогрессирования на 79% (HR=0,21; p<0,0001). Выигрыш от назначения осимертиниба наблюдался во всех анализируемых подгруппах и не зависел от предшествующего проведения адъювантной химиотерапии и стадии. Снижение относительного риска прогрессирования при IB стадии составило 50%, при II – 83%, IIIA – 88%. Данные по общей выживаемости не могут быть представлены, так как на момент анализа умер 1 пациент в группе осимертиниба и 3 в группе наблюдения.
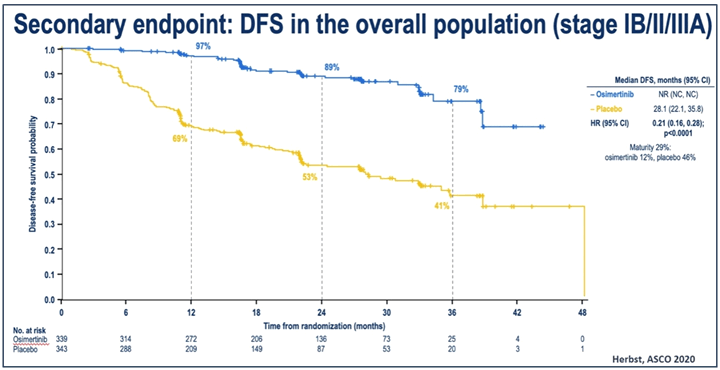
Рисунок 1. Безрецидивная выживаемость всех включенных в исследование пациентов.
Лечение осимертинибом сопровождалось умеренной токсичностью: частота осложнений 3-4 степени, обусловленных препаратом, составила 10%. Основными проявлениями токсичности преимущественно 1-2 степени были диарея (46%), паронихий (25%), кожная сыпь (26%). Отмена препарата в связи с токсичностью проведена у 11% больных, в исследовании не отмечено летальных исходов, обусловленных токсичностью.
Выдающиеся результаты были причиной расслепления больных в исследовании, в связи с чем мы, вероятно, не получим сравнительные данные по общей выживаемости. Более длительное наблюдение позволит получить показатель 5-летней общей выживаемости в группе осимертиниба и оценить, что происходит с больными после отмены приема препарата. Но уже сегодня столь большой и длительный выигрыш в безрецидивной выживаемости послужит основанием рекомендовать осимертиниб в качестве адъювантной терапии у больных НМРЛ IB-IIIA стадиями c мутацией гена EGFR после выполнения радикальной операции.
Ключевые слова: немелкоклеточный рак легкого, мутация гена EGFR, адъювантная терапия, гефитиниб, осимертиниб.
Источники: