11.03.2019

Прошедший в Сан-Франциско симпозиум ASCO «Опухоли мочеполовой системы» (GU ASCO 2019) был насыщен исследованиями, результаты которых в ближайшее время изменят подходы к лечению метастатического почечно-клеточного рака (мПКР). Больше всего изменения затронут первую линию терапии светлоклеточного мПКР.
Пембролизумаб + Акситиниб
Одним из ожидаемых сообщений было представление результатов многоцентрового рандомизированного исследования 3 фазы KEYNOTE-426 [1]. В исследовании пациенты, не получавшие ранее терапию по поводу светлоклеточного мПКР, были рандомизированы в группу ингибитора контрольных точек пембролизумаба в комбинации с таргетным препаратом акситинибом (N=432), а также в группу сунитиниба, являющегося стандартом первой линии и выбранного в качестве препарата сравнения (N=429). Пембролизумаб назначался в стандартной дозе 200 мг, внутривенно, каждые 3 недели. Акситиниб также использовался в стандартной дозе 5 мг, 2 раза в день, перорально, ежедневно, с возможностью титрации дозы до 7 и 10 мг. Сунитиниб пациенты получали в режиме 4/2.
Группы были сопоставимы по основным клиническим характеристикам. Хотелось бы описать популяцию пациентов в группе комбинированного лечения. Медиана возраста в ней составила 62 года, при этом преобладающее большинство (60%) пациентов было младше 65 лет. На 71% группа была представлена мужчинами, на 83% – пациентами с нефрэктомией в анамнезе. Только 13% больных имели неблагоприятный прогноз согласно критериям IMDC. У 73% больных более двух органов было поражено метастазами: преимущественно легкие (73%), лимфатические узлы (46%) и кости (24%). У 51 из 285 пациентов с известной архитектоникой опухоли определялись признаки саркоматоидного мПКР. Экспрессия PD-L1 не являлась критерием включения и не влияла на статистическую гипотезу. CPS (combined positive score) ≥1 (то есть наличие экспрессии PD-L1) отмечался у 59,3% больных в группе комбинации и у 61,7% – в группе сунитиниба.
Первичными конечными точками в исследовании были общая выживаемость (ОВ) и выживаемость без прогрессирования (ВБП). Дополнительные критерии включали частоту объективных ответов, длительность ответа и безопасность. Оценка проводилась независимым комитетом.
При медиане наблюдения 12,8 мес. медиана ОВ не была достигнута. Риск смерти в группе пембролизумаба-акситиниба был ниже на 47% по сравнению с сунитинибом (HR=0,53). Различия оказались достоверными (P<0,0001, рисунок 1).
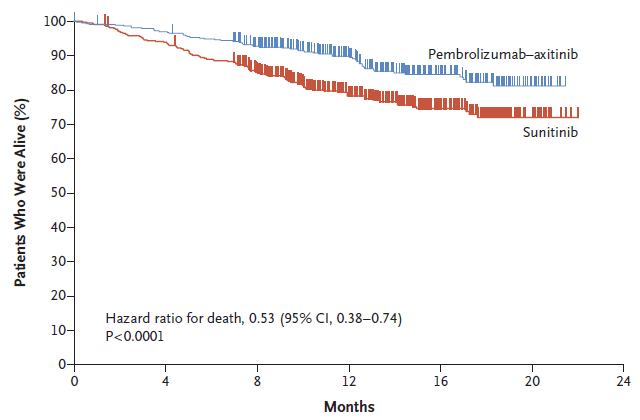
Рисунок 1. Кривые ОВ в исследовании KEYNOTE-426 (Rini et al. NEJM 2019 [2]).
Однолетняя ОВ составила 89,9% и 78,3% в этих группах, а 18-месячная ОВ – 82,3% и 72,1%, соответственно. Медиана ВБП была 15,1 мес. в группе комбинации и 11,1 мес. в группе сунитиниба (HR=0,69; P<0,001). Преимущества пембролизумаба-акситиниба наблюдались во всех подгруппах вне зависимости от прогноза пациента и статуса PD-L1. Следовательно, обе первичные конечные точки были достигнуты, исследование оказалось позитивным.
Частота ответов на лечение также выгодно отличалась в пользу комбинации (59,3% по сравнению с 35,7% для сунитиниба). 5,8% и 1,9% больных имели полные ответы, получая комбинацию и сунитиниб. Медиана длительности ответа не была достигнута в группе пембролизумаба-акситиниба и составила 15,2 мес. в контрольной группе.
По частоте развития нежелательных явлений группы не отличались. Практически у всех пациентов были зарегистрированы побочные эффекты (более 98%). Использование комбинации пембролизумаба и акситиниба сопровождалось развитием токсичности 3-4 степени у 75,8% больных, а назначение сунитиниба – у 70,6%. Наиболее частыми вариантами нежелательных явлений в группе комбинации были диарея, гипертензия, утомляемость, гипотиреоз, снижение аппетита и ладонно-подошвенный синдром. Токсичность привела к прекращению терапии одним из препаратов комбинации у 30,5% пациентов, обоими препаратами – у 10,7%. Кроме того, у 69,9% больных требовался перерыв в лечении и у 20,3% – снижение дозы.
Делая выводы, можно с уверенностью отметить высокую эффективность комбинации пембролизумаба и акситиниба у пациентов со светлоклеточным мПКР, ранее не получавших терапию. Более того, эта комбинация – прямое доказательство целесообразности сочетания ингибитора контрольных точек и таргетного препарата. Хочется напомнить, что в монотерапии пембролизумаб демонстрировал более скромные показатели. В исследовании 2 фазы KEYNOTE-427 с включением 110 пациентов частота объективных ответов составляла 38,2%, медиана ВБП – 8,7 мес. [3]. Добавление акситиниба к пембролизумабу привело к увеличению числа пациентов с ответом более чем на 20% и удлинению ВБП на 70% по сравнению с монотерапией пембролизумабом. За возросшую эффективность комбинация рассчиталась увеличенной токсичностью. Частота серьезных нежелательных явлений увеличилась в 3 раза (при монотерапии пембролизумабом была 22,7%). Однако частота отмены лечения из-за побочных эффектов уложилась в известный для терапии мПКР диапазон – 11-30%, что свидетельствует о возможности управления нежелательными явлениями комбинации.
Авелумаб + Акситиниб
Результаты исследования 3 фазы эффективности комбинации другого ингибитора контрольных точек – авелумаба и акситиниба были представлены еще на ESMO 2018 [4]. В исследовании JAVELIN Renal 101 пациенты со светлоклеточным мПКР были рандомизированы в группу авелумаба-акситиниба (N=442) или в группу сунитиниба (N=444) [5]. Главным отличием этого исследования от предыдущего было построение статистической гипотезы по оценке ВБП и ОВ в когорте пациентов, экспрессирующих PD-L1. 560 из 886 (63,2%) больных имели экспрессию PD-L1, оцениваемую как окрашивание ≥1% иммунных клеток в опухолевом образце с использованием иммуногистохимического теста SP263 (Ventana). Считается, что экспрессия PD-L1 у больных мПКР сопряжена с худшим прогнозом и снижением эффективности таргетной терапии.
На GU ASCO 2019 были представлены новые результаты эффективности комбинации в различных подгруппах. Прежде всего хочется отметить, что первичная конечная точка – ВБП – была достигнута: медиана ВБП составила 13,8 мес. в экспериментальной группе и 7,2 мес. – в контрольной (P<0,001, рисунок 2).
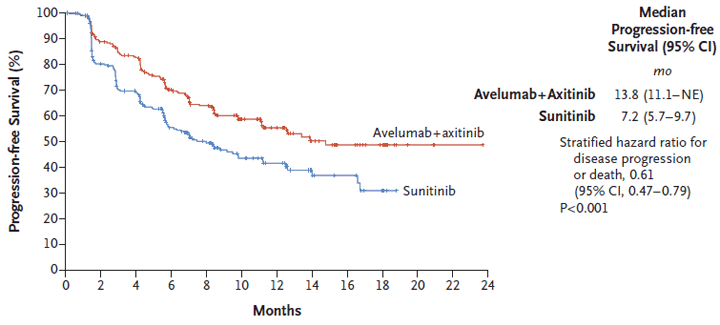
Рисунок 2. Кривые ВБП в группах пациентов с PD-L1 экспрессией
в исследовании JAVELIN Renal 101 (Motzer et al. NEJM 2019 [6]).
Что вызвало интерес, так это сохранившиеся различия по данному параметру и в общей когорте пациентов (как с экспрессией PD-L1, так и без): 13,8 мес. и 8,4 мес. для авелумаба-акситиниба и сунитиниба соответственно (P<0,001). Медиана ОВ – вторая главная конечная точка – в настоящее время в группах не достигнута и наблюдение продолжается.
Частота объективных ответов у пациентов с экспрессией PD-L1 была в 2 раза лучше в группе комбинированного лечения – 55,2% по сравнению с 25,5% для сунитиниба. Существенные различия также отмечались и в общей когорте – 51,4% и 25,7%. Полные ответы были зарегистрированы у 4,4% больных, получавших авелумаб-акситиниб, и у 2,1% получавших сунитиниб. Все объективные ответы оказались длительными, медиана не была достигнута.
Важнейшим моментом стала оценка эффективности комбинации в зависимости от прогноза по критериям IMDC и MSKCC. Комбинация двух препаратов сохранила свое превосходство над сунитинибом во всех прогностических группах. Однако ради справедливости нужно отметить, что пациентов с плохим прогнозом было не так много –
Если посмотреть на профиль токсичности комбинации, то снова нежелательные явления всех степеней были отмечены у 99,5% больных, а частота нежелательных явлений 3 степени и выше составила 71,2%. Профиль токсичности очень похож на профиль комбинации пембролизумаба-акситиниба. В группе авелумаба-акситиниба также наиболее часто встречались диарея, гипертензия, утомляемость, тошнота, ладонно-подошвенный синдром. У 7,6% больных пришлось отменить оба препарата из-за токсичности. Однако 10,8% пациентов имели даже эскалацию дозы акситиниба.
Таким образом, комбинация авелумаба и акситиниба показала значительные преимущества по сравнению с сунитинибом в когортах не получавших ранее терапию пациентов со светлоклеточным мПКР, как экспрессирующих PD-L1, так и вне зависимости от экспрессии PD-L1. Приведенные факты равной эффективности комбинации в группах с и без PD-L1 экспрессии являются интересными, но вряд ли стоит экстраполировать их на генеральную совокупность – ведь исследование было статистически спланировано доказать различия по основным точкам только в когорте экспрессирующих больных, а, следовательно, с позиций доказательной медицины мы не имеем достаточных оснований использовать препараты у всех пациентов, без знания уровня экспрессии. С другой стороны, стало совершенно очевидно, что назначение таргетных препаратов в монотерапии у пациентов с экспрессией PD-L1 не приводит к позитивному эффекту. Вот уже не в первый раз в этой когорте больных сунитиниб показывает медиану ВБП 7 мес. Те же цифры демонстрировались в исследовании IMMOTION 151 [7].
Ниволумаб + Ипилимумаб
Наконец, результаты 30-месячного наблюдения в исследовании CheckMate 214, в котором изучалась эффективность комбинации ниволумаба и ипилимумаба у пациентов с мПКР и промежуточным/плохим прогнозом, ранее не получавших терапию, были представлены на симпозиуме [8]. Комбинация продемонстрировала достоверные преимущества по общей выживаемости и частоте ответов по сравнению с сунитинибом, о чем писали ранее [9]. В настоящий момент комбинация ниволумаба и ипилимумаба наиболее близка к практическому использованию в России, так как была официально зарегистрирована для применения. Эта лечебная опция уже добавлена в практические рекомендации NCCN [10] и новую версию рекомендаций ESMO [11] как стандарт с наивысшим уровнем доказательности 1.
Отдаленные результаты эффективности и токсичности представляют большой интерес, отражая длительное воздействие на исходы. Медиана продолжительности жизни в группе комбинации так и не была достигнута – более 50% больных живы. В группе сунитиниба этот показатель составил 26,6 мес. Различия оказались существенными (HR=0,63; P<0,0001). 2-летняя ОВ составила 66% и 53% соответственно. Частота объективных ответов была как в абсолютных цифрах (42% по сравнению с 29%), так и статистически (P=0,0001) лучше при терапии ниволумабом и ипилимумабом. Представить раньше, что 11% таких прогностически тяжелых пациентов будут иметь полные ответы, то есть когда все метастазы исчезают, было сложно. Теперь это реальность.
В течение 30 месяцев число нежелательных явлений в группе комбинации существенно не изменилось. Так, 5 дополнительных пациентов, получавших комбинацию, и 7 пациентов, получавших сунитиниб, имели нежелательные явления 3-4 степени, при этом только у 1 и 3 пациентов из этих групп терапия была прервана из-за токсичности.
Значительным прорывом можно считать появление новой опции терапии пациентов с промежуточным и плохим прогнозом. Для последней группы лишь темсиролимус имел наивысшую категорию доказательности, обеспечивая медиану ОВ в 10,9 мес. [12]. Комбинация ниволумаба и ипилимумаба снижает риск смерти на 37% по сравнению с сунитинибом. Долгосрочное наблюдение за больными, получавшими комбинацию двух ингибиторов контрольных точек, подтверждает ее эффективность. Использование ипилимумаба в низкой дозе (1 мг/кг) привело к умеренной токсичности комбинации без потери эффективности. Качество жизни пациентов, получающих комбинацию, было также значимо лучшим; симптомы болезни регистрировались реже у этих пациентов [13].
Сравнение эффективности комбинаций.
Возможный алгоритм назначения препаратов в будущем
Итак, 3 новые комбинации входят в первую линию терапии светлоклеточного мПКР. Возникает вопрос, можно ли сравнивать эффективность этих комбинаций? Сопоставить цифры достаточно просто, но, с моей точки зрения, делать это не совсем правильно. Комбинация пембролизумаба/акситиниба изучалась в общей когорте больных вне зависимости от статуса экспрессии PD-L1. Комбинация авелумаба/акситиниба изучалась у пациентов с экспрессией PD-L1, что изменяет течение болезни. Обе комбинации достаточно хорошо изучены в группах благоприятного и промежуточного прогноза и недостаточно – в группе плохого прогноза (только 13% и 12% больных с плохим прогнозом включены в соответствующие исследования). Комбинация ниволумаба/ипилимумаба, наоборот, изучалась у пациентов с промежуточным и плохим прогнозом, но без оглядки на экспрессию PD-L1 как определяющий фактор.
Таким образом, картина складывается удачно: появление трех комбинаций позволит персонализировать терапию. Предположу следующий алгоритм (рисунок 3). На первом этапе всем пациентам со светлоклеточным раком определяется экспрессия PD-L1. В случае экспрессии пациентам назначается комбинация авелумаба и акситиниба. У пациентов с отсутствием экспрессии оценивается прогноз. При благоприятном прогнозе показанием будет комбинация пембролизумаба и акситиниба, при плохом – ниволумаба и ипилимумаба. При промежуточном прогнозе обе комбинации могут быть назначены пациенту. Таргетные препараты в монорежимах переместятся из первой линии в последующие.
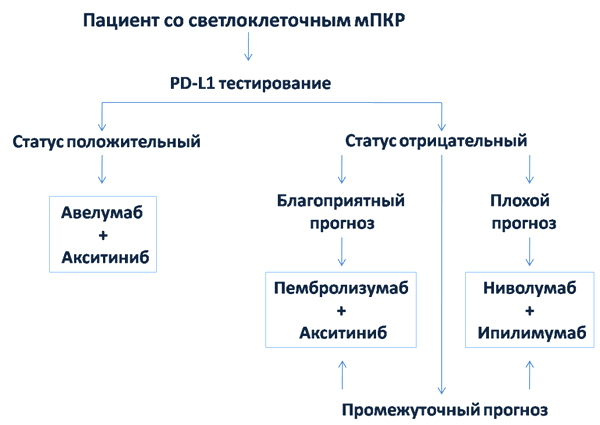
Рисунок 3. Возможный алгоритм назначения препаратов в первой линии терапии мПКР.
Литература: