21.12.2016
Сингапур, 18 декабря 2016

Создание препаратов нового класса аллостерических ингибиторов рецептора фактора роста фибробластов 2 типа (FGFR2) позволит увеличить эффективность и существенно снизить токсичность терапии злокачественных опухолей. Результаты российского исследования эффективности и безопасности первого аллостерического ингибитора FGFR2 алофаниба были представлены в виде устного доклада на конгрессе Европейского общества медицинской онкологии (ESMO Asia 2016), который состоялся в Сингапуре 16-19 декабря 2016 (Abstract 151O).
Результаты исследований
Алофаниб относится к низкомолекулярным химическим соединениям. В отличие от ингибиторов тирозинкиназы препарат избирательно связывается с надмембранной частью FGFR2, не взаимодействуя с киназами и другими рецепторами.
В исследованиях in vitro алофаниб угнетал пролиферацию клеток трижды негативного рака молочной железы и рака яичников, экспрессирующих FGFR2, в отличие от клеток меланомы, на которых экспрессия рецептора не определялась. Механизм угнетения пролиферации был связан с активацией в клетках апоптоза в результате блокирования FGFR2.
Нестабильность генома опухолевой клетки приводит к появлению различных изоформ FGFR2, что снижает эффективность терапии, например, моноклональными антителами. Алофаниб ингибировал главные изоформы FGFR2 – IIIc и IIIb, тем самым преодолевая данный механизм устойчивости.
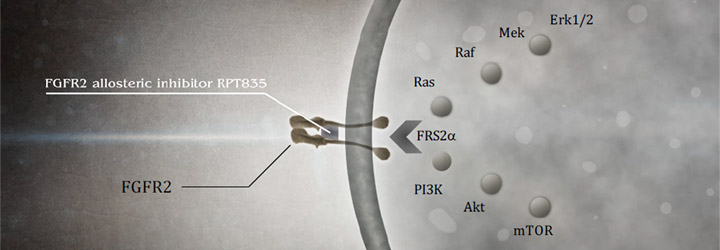
Блокада рецептора препятствует распространению сигнала в опухолевую клетку. Так, после культивации клеток с алофанибом первый внутриклеточный белок в сигнальном пути – FRS2a – оказался неактивным. Ингибирующая концентрация (IC50) составила 7 нмоль/л.
Алофаниб достоверно ингибирует ангиогенез. Пролиферация эндотелиальных клеток, возможность миграции, образование сосудисто-подобных структур и зрелых сосудов были подавлены алофанибом. Бевацизумаб, как препарат сравнения, не оказался активным в модели FGF-стимулированного ангиогенеза. Следовательно, в случае развития резистентности к терапии, направленной на рецептор фактора роста эндотелия сосудов (VEGFR), одним из вариантов последующей терапии может быть ингибитор FGFR.
В исследованиях на животных было продемонстрировано, что алофаниб тормозит рост опухолей. Эффект терапии зависел от дозы и экспрессии FGFR2. Например, лучшие результаты были достигнуты для трижды негативного рака молочной железы с максимальной экспрессией FGFR2.
В настоящее время появились первые сведения о значении пути FGFR2 в развитии рака яичников. 17% больных раком яичников имеют амплификацию FGFR2. Предполагается, что комбинация традиционных химиотерапевтических режимов на основе препаратов платины с ингибиторами FGFR2 позволит увеличить эффективность лечения. В представленном доклиническом исследовании комбинация паклитаксела и карбоплатина с алофанибом привела к торможению роста опухоли на 80%. При изучении структуры опухоли в группе алофаниба были найдены обширные некрозы и клеточная дегенерация, индекс Ki-67 был достоверно снижен, и снова было выявлено угнетение роста сосудов. Патоморфологические изменения в группе только химиотерапии не наблюдались.
В исследованиях острой и хронической токсичности введение алофаниба хорошо переносилось животными. LD50 составила 1650 мг/кг. Смертей, связанных с лечением, серьезной гематологической токсичности и органных нарушений на протяжении 6 месяцев терапии исследователи не выявили.
Гиперфосфатемия – тяжелый побочный эффект, встречаемый часто при изучении ингибиторов тирозинкиназы FGFR1-3. Алофаниб, как селективный ингибитор FGFR2, не приводил к изменению уровня фосфатов в крови. В исследовании был зарегистрирован новый вид токсичности – угнетение сперматогенеза. Сперматоциты экспрессируют FGFR2. Ингибирование FGFR2 алофанибом, по-видимому, приводит к подавлению сперматогенеза. И, наконец, воспаление стенки сосудов – хорошо известный побочный эффект всех антиангиогенных препаратов, также характерный для алофаниба.
Главные выводы
«Алофаниб является селективным низкомолекулярным аллостерическим ингибитором FGFR2. В доклинических исследованиях алофаниб продемонстрировал невысокую токсичность и значительную эффективность, особенно в случае терапии опухолей с экспрессией FGFR2. Протокол клинического исследования 1b фазы алофаниба прошел конкурсный отбор и был разработан на европейском курсе клинических исследований ECCO-AACR-EORTC-ESMO. Исследование начнется в начале 2017 года», – сделал вывод Илья Тимофеев, представлявший доклад на конгрессе ESMO Asia.

«FGFR2 представляется принципиальной мишенью таргетной терапии. Рецептор играет важную роль в патогенезе, например, таких опухолей, как рак желудка, рак тела матки, рак молочной железы. Применение нового класса высокоселективных ингибиторов FGFR2 может быть эффективным и хорошо переносимым у пациентов с метастатическим раком», – заключил в обсуждении Olivier Rixe, профессор и ассоциированный директор по клиническим исследованиям Онкологического Центра Университета Нью-Мексико (США).
Публикации
Результаты доклинических исследований были опубликованы в международных журналах.