23.05.2016

18 мая 2016 года Управление по контролю над качеством пищевых продуктов и лекарственных средств США (FDA) по результатам клинического исследования 2 фазы одобрило комбинацию ленватиниба и эверолимуса для применения у пациентов с метастатическим почечно-клеточным раком (мПКР), которые прогрессировали на предшествующей таргетной терапии, направленной против семейства фактора роста эндотелия сосудов (VEGF).
Одобрение FDA после исследования 2 фазы уже свидетельствует о чем-то неординарном. Действительно, впервые у больных с устойчивым к таргетной терапии мПКР была достигнута выживаемость без прогрессирования более года, медиана общей выживаемости превысила 2 года, а частота объективных ответов составила 43%. Впервые для рака почки была зарегистрирована комбинация двух таргетных препаратов, оказавшаяся более эффективной, чем каждый препарат в отдельности. И, главное, впервые использование двух препаратов привело к блокированию ключевых, известных на данный момент механизмов резистентности рака почки к ингибиторам VEGF/VEGFR, которые включают активацию альтернативных путей, недостаточное ингибирование рецептора VEGF и активацию внутриклеточных киназ.
Ленватиниб является селективным ингибитором VEGFR1-3. Следовательно, при развитии устойчивости к препаратам предшествующей терапии, связанной с недостаточным ингибированием VEGFR1-3 на клетках опухоли или на клетках сосудов, целесообразно использовать более селективный ингибитор, подавляющий активность рецепторов.
Кроме того, ленватиниб в наномолярной концентрации блокирует рецепторы фактора роста фибробластов (FGFR) и, прежде всего, FGFR1.
Большинство авторов объясняет резистентность рака почки активацией параллельных патогенетических путей в клетках ПКР и эндотелиоцитах или появлением активирующих мутаций [1-3]. Патогенетический путь фактора роста фибробластов (FGF) и его рецепторов представляется альтернативным в проведении сигнала в клетку и играет важную роль в устойчивости ПКР к лекарственному лечению.
Экспрессия FGFR1 была выявлена в 98% случаев на клетках первичной опухоли почки и в 82,5% случаев на клетках метастазов ПКР в лимфатические узлы [4]. Во всех случаях интенсивность окрашивания при иммуногистохимическом анализе была высокой (3+), что свидетельствует о сильной экспрессии рецептора. Экспрессия FGFR1 на клетках неизмененной ткани почки была выявлена только в 1 случае (2,5%). Отличия с ПКР оказались высоко достоверными (P=0,001).
В многофакторном анализе изучалось влияние экспрессии FGFR1 на выживаемость без прогрессирования пациентов с мПКР, получающих таргетную терапию сорафенибом [5]. В исследование было включено 40 пациентов. У пациентов с экспрессией FGFR1 отмечено снижение показателей выживаемости без прогрессирования (P=0,04).
Установлено, что в крови здоровых людей уровни FGF-1 и FGF-2 были достоверно ниже по сравнению с больными мПКР. Наибольшие различия были продемонстрированы для FGF-2 (P=0,00033) [6]. Повышение концентрации FGF-2 более чем в 2 раза в крови больных мПКР отмечается перед прогрессированием на сунитинибе [7].
В другом исследовании у 38 больных мПКР была проанализирована концентрация в плазме FGF-2 и VEGF-A, как основных факторов, обладающих проангиогенной активностью, до начала и в процессе терапии сунитинибом [8]. У пациентов с прогрессированием болезни после двух циклов лечения сунитинибом было выявлено достоверное повышение концентрации FGF-2 в плазме (P=0,001), при этом у пациентов, которые имели ответ на лечение или стабилизацию болезни, изменений в уровне FGF-2 не было (P=0,2). Концентрация VEGF-A достоверно увеличилась у пациентов с ответом на лечение сунитинибом (P=0,033), что является известным благоприятным фактором. Изменений в уровне VEGF-A у пациентов с прогрессированием не выявлено (P=0,8). Таким образом, результаты этого исследования свидетельствуют о том, что увеличение концентрации FGF-2 возможно является предиктором прогрессирования болезни у пациентов, получающих анти-VEGF терапию (в частности, сунитиниб), а повышение уровня VEGF-A может указывать на благоприятное течение болезни.
Еще в одной работе методом Вестерн-блот оценивалось содержание FGF-2 в ткани здоровой почки, в почечно-клеточном раке, а также в сальнике [9]. Наибольшее содержание FGF-2 было обнаружено в опухоли почки по сравнению со здоровой тканью почки (p<0,05). Кроме того, FGF-2 ткани сальника и рака почки имел большую митогенную (96%, 68%, 38%, p<0,05) и ангиогенную (5,5, 2,7 и 1,6 сосудов, p<0,05) активность. Авторы предполагают, что FGF-2 может обладать аутокринным действием при развитии рака почки.
Негативная роль FGF в развитии метастазов ПКР в костях (через активацию васкуляризации) описывалась в нескольких публикациях [10, 11].
FGFR1 в отличие от других рецепторов FGF сильно экспрессирован на эндотелиальных клетках [12, 13]. Экспериментальные данные свидетельствуют о значении пути FGF/FGFR1 в развитии сосудов в опухоли [14, 15]. FGFR1, лиганды FGF-1,2,4,8,10 корецепторы FGFR1 (например, синдекан-4) играют одну из важнейших ролей на всех этапах формирования сосуда: активации эндотелиальных клеток, миграции эндотелиальных клеток в опухоль, пролиферации эндотелиоцитов в опухоли через активацию внутриклеточных путей MAPK и PKC, образовании тубулярных структур и затем зрелых сосудов [16-20]. Более того, существуют сведения, что FGF-2 оказывает перекрестное действие и повышает экспрессию VEGFR и VEGF на эндотелиальных клетках [21, 22].
В моделях стимуляции ангиогенеза фактором роста фибробластов (FGF) сунитиниб и бевацизумаб не смогли подавить рост новых сосудов (P=0,2 и P=0,85 соответственно) [23]. В моделях стимуляции ангиогенеза фактором роста эндотелия сосудов (VEGF) сунитиниб и бевацизумаб достоверно ингибировали рост новых сосудов (P=0,001 и P=0,001). Отличий между препаратами не было. Результаты настоящего исследования демонстрируют, что анти-VEGF терапия достоверно влияет на VEGF-индуцированный ангиогенез и не влияет на FGF-индуцированный рост сосудов.
Основываясь на результатах фундаментальных исследований, демонстрирующих значимость пути FGF/FGFR1 в развитии ПКР и других опухолей, несколько компаний приступили к разработке препаратов, блокирующих этот путь. Ленватиниб – первый зарегистрированный препарат для лечения мПКР, ингибирующий тирозинкиназу FGFR1 и тем самым блокирующий проведение сигнала через путь FGF/FGFR1 в клетках рака почки [24].
Хорошо известно, что активация внутриклеточных киназ может не зависеть от активности клеточного рецептора. Другими словами, рецепторы на поверхности клетки заблокированы, но это не приводит к подавлению сигнала внутри клетки. В связи с этим представляется целесообразным использовать ингибиторы внутриклеточных киназ, одним из которых является эверолимус. Эверолимус ингибирует белок mTOR, который близко расположен к ядру. Ранее было показано, что mTOR активирован в клетках рака почки [25]. Ингбирование mTOR препятствует распространению сигнала в ядро.
Таким образом, применение комбинации ленватиниба и эверолимуса приводит к дезактивации патогенетически значимых путей – VEGFR, FGFR и mTOR.
Одобрение FDA было основано на результатах рандомизированного исследования 2 фазы [26,27], в котором 153 пациента с мПКР и прогрессированием на предшествующей таргетной анти-VEGF терапии были распределены в соотношении 1:1:1 в группы:
Главным критерием эффективности была выживаемость без прогрессирования (ВБП). Оценка ответа проводилась каждые 8 недель на основании критериев RECIST 1.1.
Количество пациентов с плохим прогнозом согласно модели MSKCC составляло 20%, 23% и 38% в группах комбинации, ленватиниба и эверолимуса. 86%, 83% и 96% пациентов имели нефрэктомию в анамнезе соответственно. В исследовании принимали участие пациенты со светлоклеточным ПКР.
Применение ленватиниба в комбинации с эверолимусом достоверно увеличивало ВБП по сравнению с эверолимусом в монотерапии – 14,5 мес. (95% ДИ 5,9–20,1) против 5,5 мес. (95% ДИ 3,5–7,1; HR=0,40, p=0,0005). Статистически значимых различий в медиане ВБП между комбинацией и ленватинибом (7,4 мес., 95% ДИ 5,6–10,2) не было (HR=0,66, p=0,12).
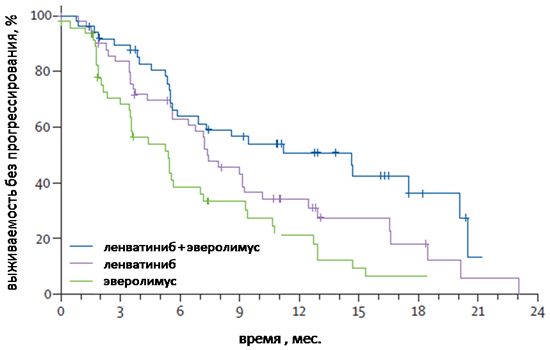
Рисунок 1. Выживаемость без прогрессирования.
Наилучшая частота объективных ответов была достигнута в группе комбинации (43%) по сравнению с группой ленватиниба (27%, P=0,0067) и группой эверолимуса (6%, P<0,0001).
Медиана общей выживаемости составила 25,5 мес. в группе левнатиниб+эверолимус и была достоверно лучше, чем в группе эверолимуса (15,4 мес., P=0,024). Достоверных отличий в общей выживаемости между группой ленватиниба (19,1 мес.) и группой эверолимуса не было (P=0,12).
Частота всех нежелательных явлений 3/4 степени токсичности в группе комбинации была 57%/14%, в группе монотерапии ленватинибом – 73%/6% и в группе монотерапии эверолимусом – 42%/8%. Наиболее частыми побочными эффектами у пациентов, получающих комбинацию препаратов, были диарея, снижение аппетита и утомляемость. Отмена терапии из-за токсичности происходила у 24% больных, получающих комбинацию, 25% больных на ленватинибе и 12% – на эверолимусе.
Применение эффективной комбинации ленватиниба и эверолимуса в практике приведет к расширению арсенала онколога в борьбе с мПКР, позволит планировать еще одну линию терапии при прогрессировании на стандартных препаратах, блокирующих путь VEGF/VEGFR, и отразится на показателях продолжительности жизни пациентов в реальной жизни.
Литература: