25.03.2016
Тошнота и рвота до сих пор остаются наиболее частыми и нежелательными осложнениями при проведении современной химиотерапии и лучевой терапии [1-3]. В отличие от исследований, направленных на изучение механизмов развития тошноты и рвоты, индуцированных химиотерапией, прогресс в изучении подобных осложнений, обусловленных проведением лучевой терапии, крайне незначителен. Среди факторов риска возникновения тошноты и рвоты, ассоциированных с лучевой терапией, чаще всего называют область облучения (брюшная полость), размер поля облучения (>400 см2) и проведение химиотерапии (как самостоятельного метода лечения до проведения лучевой терапии или как сопроводительного метода лечения в момент проведения лучевой терапии) [3].
В ряде исследований было показано, что комбинация таких антагонистов рецепторов нейрокинина-1 (NK-1), как апрепитант, нетупитант, ролапитант с антагонистами рецепторов 5-гидрокситриптамина-3 (5-HT3) и дексаметазоном, способствует предотвращению развития тошноты и рвоты у больных, получающих высоко или умеренно эметогенную химиотерапию, в течение первых 10 часов после начала ее проведения [4-13]. Лишь в одном небольшом рандомизированном исследовании, в котором приняли участие 40 человек, была изучена возможность антагонистов рецепторов NK-1 предотвращать развитие тошноты и рвоты, индуцированных проведением лучевой терапии [14]. Как бы то ни было, недостатками последнего исследования являлось то, что лишь 24 пациента из 40 участников исследования получали сочетанное химиолучевое лечение, дозы препаратов и эметогенность терапии не были описаны. Более того, во время проведения исследования больные не получали кортикостероиды. Таким образом, до сегодняшнего дня не существовало ни одного рандомизированного исследования, целью которого являлось бы изучение профилактики тошноты и рвоты на протяжении всех 5 недель проведения сочетанного курса химиолучевой терапии.
В одном из исследований 2 фазы, проведенном у больных онкогинекологическими заболеваниями, получающих лучевую терапию в сочетании с еженедельными введениями цисплатина и сопроводительную антиэметогенную терапию палоносетроном и преднизолоном, было показано, что 57% пациентов завершили полностью данный 5-недельный курс лечения без развития тошноты и рвоты [15]. Опыт успешного применения антиэметогенных препаратов для профилактики тошноты и рвоты, индуцированных химиотерапией, позволил предположить, что проведение сопроводительной терапии антагонистами рецепторов NK-1 и 5-HT3 и дексаметазоном позволит лучше справляться с данными осложнениями при проведении сочетанного химиолучевого лечения. В одном из наблюдательных исследований, проведенном у пациентов, получающих сочетанную химиолучевую терапию, было выполнено сравнение между двумя режимами профилактики тошноты и рвоты (антагонист рецепторов 5-HT3 и дексаметазон ± апрепитант) [16]. По результатам данного исследования в группе больных, получавших апрепитант, на 15% больше больных не испытывали тошноту или не применяли дополнительные антиэметики в течение первых 120 часов после начала лечения.
Фосапрепитант является пролекарственной формой селективного высокоаффинного антагониста рецепторов NK-1 апрепитанта. После внутривенного введения фосапрепитант быстро метаболизируется до апрепитанта. Однократное введение 150 мг фосапрепитанта до начала проведения химиотерапии соответствует 3 дням таблетированного приема апрепитанта [17]. Целью опубликованного недавно в The Lancet Oncology двойного слепого рандомизированного исследования 3 фазы было изучить, насколько добавление фосапрепитанта к палоносетрону и дексаметазону способствует профилактике тошноты и рвоты у больных раком шейки матки при проведении у них сочетанного курса 5-недельной лучевой терапии и еженедельной терапии цисплатином в дозе 40 мг/м2 [18].
В этом исследовании, длившемся с июня 2010 г. по март 2015 г., приняли участие 234 больных раком шейки матки. Всем больным должна была быть проведена лучевая терапия на область малого таза (РОД 1,8-2,0 Гр, 5 дней в неделю) в сочетании с еженедельным введением цисплатина в дозе 40 мг/м2. Лечение выполнялось в течение 5 недель. В исследование не включались пациенты, получившие химиотерапию или лучевую терапию по поводу основного заболевания. Все участники исследования были рандомизированы в соотношении 1:1 в две группы, одна из которых получала до введения цисплатина фосапрепитант (150 мг в/в), а вторая – плацебо в комбинации с палоносетроном (0,25 мг в/в) и дексаметазоном (16 мг перорально). Дексаметазон назначался в дозе 8 мг × 2 р/д во 2-й день, 4 мг × 2 р/д в 3-й день и 4 мг × 1 р/д в 4-й день.
Основным критерием эффективности был процент пациентов, у которых не развилась рвота в течение всего периода лечения.
Из 234 пациентов, принявших участие в исследовании, 118 получали фосапрепитант и 116 – плацебо. По результатам данного исследования 48,7% больных, получавших плацебо (95% ДИ 25,2-72,2), и 65,7% больных, получавших фосапрепитант (95% ДИ 42,2-89,2), не испытывали рвоту к 5-й неделе лечения (рис. 1).
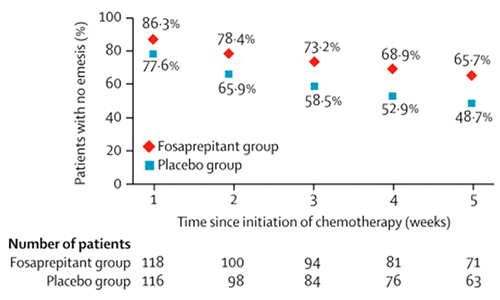
Рисунок 1. Процент пациентов, у которых не развилась рвота на протяжении 5 недель
сочетанной лучевой терапии и еженедельных введений цисплатина.
Кумулятивный риск развития рвоты в группе больных, получавших фосапрепитант, был значительно ниже по сравнению с контрольной группой (p=0,008). В обеих группах больные переносили лечение удовлетворительно, а развившиеся нежелательные явления 3 степени не были связаны с изучаемой комбинацией антиэметогенных препаратов.
Данное исследование явилось первой работой, авторы которой изучили эффективность и безопасность применения антагонистов рецепторов NK-1 на протяжении 5 недель проведения сочетанной лучевой терапии и еженедельной химиотерапии цисплатином. Пациенты, получавшие фосапрепитант в комбинации с палоносетроном и дексаметазоном, меньше испытывали тошноту и рвоту по сравнению с больными, получавшими только сопроводительную антиэметогенную терапию палоносетроном и дексаметазоном. Изучаемая комбинация антиэметиков удовлетворительно переносилась. Как бы то ни было, проведение дополнительных исследований, направленных на изучение профилактики тошноты и рвоты у больных, получающих сочетанное химиолучевое лечение, необходимо для подтверждения полученных результатов.
Литература: