СКРИНИНГ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ
В.Ф. Семиглазов
ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург
Из 10 млн. новых случаев злокачественных опухолей различных органов, выявляемых в мире, 10% приходится на молочную железу. Если оценивать только женскую популяцию удельный вес рака полочной железы (РМЖ) возрастает до 22%. В промышленно развитых странах удельный вес РМЖ еще выше – 27%. Но РМЖ - также наиболее часто встречающаяся опухоль и в развивающихся странах. В 2000 г. РМЖ выявлен у 471 тыс. женщин развивающихся стран, т.е. чаще, чем рак шейки матки (379 тыс.), лидировавший в предшествующие годы.
Более половины случаев РМЖ (579 тыс.) ежегодно регистрируется в Северной Америке, Западной Европе, Австралии и Новой Зеландии, где РМЖ возникает у 6% женщин на протяжении жизни (до 75 лет). Такая же частота этих опухолей в Аргентине и Уругвае. Самая низкая частота РМЖ наблюдается в Африке (южнее Сахары), Юго-восточной Азии и Японии, где вероятность заболеть РМЖ составляет одну треть по сравнению с Западом (у 2% женщин на протяжении жизни до 75 лет). Российская Федерация и страны Центральной и Восточной Европы занимают по частоте РМЖ промежуточное положение. В Российской Федерации ежегодно выявляется около 47 тыс. новых случаев РМЖ. (В.Ф. Семиглазов, 2001).
До 1980-х гг. наблюдался рост заболеваемости и смертности как в экономически развитых, так и в развивающихся странах. Далее, по мере внедрения маммографического скрининга и улучшения прогноза выявленных случаев РМЖ в экономически развитых странах Запада произошли значительные изменения этих показателей с замедлением, а затем и снижением показателей смертности (IARC, 2002). В странах Восточной Европы и Латинской Америки, наоборот, продолжился рост заболеваемости и смертности от РМЖ.
В 1990 г. показатели заболеваемости отличались приблизительно в 8 раз, отражая особенности этиологии РМЖ в различных частях мира. Изучение географической вариабельности и тенденций заболеваемости РМЖ, а также последствий миграции популяции из стран с низкой заболеваемостью в страны с высокой заболеваемостью РМЖ позволяет выявить важную роль внешних факторов в этиологии заболевания. Известно, что низкая рождаемость, поздний возраст первых родов, раннее наступление менструальной функции и поздняя менопауза – факторы, ассоциирующиеся с увеличением риска РМЖ. Тенденция к снижению показателей репродукции в западных популяциях частично объясняет нарастание частоты РМЖ.
Широкое распространение маммографического скрининга в ряде стран изменило соотношение удаляемых доброкачественных и злокачественных опухолей молочной железы. В особенности драматически возросла частота неинвазивного РМЖ (карциномы in situ), что вызывает постоянные дебаты об оптимальном лечении таких «начальных» форм рака. В то время как конечная цель скрининга – сократить смертность от РМЖ, немедленная его цель заключается в обнаружении рака до клинического проявления. В то же время обнаружение рака (или его предшественников) до клинического проявления повышает риск ложноположительной диагностики и избыточного лечения.
РМЖ – гетерогенное заболевание, характеризующееся различной «естественной историей». Распространенный взгляд о том, что эпителиальная опухоль молочной железы неизбежно прогрессирует от атипии к карциноме in situ, далее - к инвазивному раку и последующему метастазированию поддерживается далеко не всеми исследователями (Buerger, 2001). Протоковая и дольковая эпителиальная пролиферация, особенно с атипией, несомненно, увеличивают риск РМЖ (ОР=2-4). Однако эти заболевания, скорее всего, определяют лишь часть спектра заболеваемости РМЖ. Возможно, что эта патология не является базисом для развития всех форм РМЖ. Поскольку скрининговая маммография, в отличие от клинического метода (пальпации), позволяет рано выявить разнообразную патологию молочной железы, становится особенно важным знать больше о риске прогрессии различных видов и форм идентифицированной патологии. Понимание угрозы и частоты прогрессии этой патологии критически важно при проведении программы скрининга, включая и выбор адекватного лечения выявленного заболевания.
Молекулярно-генетические исследования DCIS (протоковой карциномы in situ) и атипической протоковой гиперплазии методом «потери гетерозиготности» показали схожие генетические повреждения, свидетельствующие о клональном происхождении этих заболеваний (Lakhani, 1995). Кроме того, было показано, что неинвазивные (in situ) и инвазивные структуры РМЖ имеют идентичные молекулярно-генетические изменения, т.е. являются ступенями одного и того же патогенетического пути (Stratton, 1995). Эти находки совпадают с наблюдениями о схожести морфологической характеристики in situ и инвазивного компонента рака (Lampejo, 1994). Эта концепция в определенной мере совпадает с гипотезой о том, что рак in situ низкой степени злокачественности превращается в инвазивный рак также низкой степени злокачественности, и, наоборот, рак in situ высокой степени злокачественности прогрессирует в инвазивный рак высокой степени злокачественности. Данные Шведского проекта скрининга дали основание для альтернативной гипотезы. По мнению Tabar (1992), опухоль прогрессирует от низкой к высокой злокачественности, а пропорция опухолей высокой степени злокачественности увеличивается с нарастанием размера опухоли.
Недавние исследования DCIS с использованием методики геномной гибридизации дали возможность сформулировать модель патогенеза DCIS (Buerger, 1999). Выяснилось, что различные морфологические классы DCIS имеют специфические генетические изменения, не встречающиеся при других вариантах. Хорошо дифференцированная DCIS ассоциируется с потерей аллелей 16q и 17q, в то время как опухоли промежуточной и высокой степеней злокачественности имеют потери значительно большего числа аллельных хромосомных ветвей (Fujii, 1996; Chuaqui, 1997). Схожие изменения при атипической дольковой гиперплазии и дольковой карциноме in situ выражаются в подобных генетических мутациях с потерей материала от 16р, 16q, 17q, 22q (Lu, 1998). Хотя DCIS низкой степени злокачественности и атипическая протоковая гиперплазия не имеют генетической схожести с DCIS высокой степени злокачественности, они имеют заметную схожесть с дольковой карциномой in situ и атипической дольковой гиперплазией. Эти наблюдения ставят под сомнение существующее мнение о том, что дольковая и протоковая карциномы in situ являются различными заболеваниями, а DCIS – гомогенным процессом. Будущие молекулярные маркеры обеспечат лучшую дискриминанту морфологических схожих опухолевых образований.
Скрининг выявляет широкий спектр опухолей, ранжируемый от микрофокусов DCIS низкой степени злокачественности до крупных инвазивных РМЖ. Предполагается, что обнаружение рака in situ (особенно, высокой степени злокачественности) предотвращает развитие инвазивного рака высокой степени злокачественности (основной причины летального исхода). Хорошо известно, что многие инвазивные РМЖ низкой степени злокачественности также идентифицируются при скрининге. Такие опухоли характеризуются хорошим прогнозом, но, будучи индолентными (медленно прогрессирующими), могут никогда не проявиться клинически на протяжении жизни пациента. Скрининг в этих случаях приносит вред пациенту. Определенная пропорция этих опухолей (как полагает Tabar, 1999) может на протяжении времени дедифференцироваться в более агрессивные опухоли. Это, однако, не обнаружено в Финской программе маммографического скрининга (Hakama, 1995). Все же надо считать, что идентификация и удаление таких опухолей позволяет избежать их потенциальной способности к прогрессии. Обнаружение инвазивного рака высокой степени злокачественности путем скрининга, когда опухоль еще не определяется клиническим исследованием (пальпацией), означает возможность снизить смертность от РМЖ. Подтверждением этого являются результаты Шведского скрининга, в котором опухоли 3-й степени злокачественности, но минимального размера (менее 1 см) имели все же благоприятный прогноз и были излечены (Tabar, 1999).
Протоковые раки, составляющие большинство опухолей молочной железы, характеризуются время-зависимыми прогностическими факторами (размер опухоли, статус лимфоузлов), свидетельствующими о возможной эффективности скрининга (например, при минимальном размере опухоли и отсутствии регионарных метастазов). Дольковые же раки или смешанные опухоли, включающие дольковые структуры, как правило, являются более крупными с нередким поражением лимфатических узлов ко времени их маммографического выявления. Поэтому то идентификация РМЖ с дольковым компонентом в скрининге не приносит существенной пользы с точки зрения снижения смертности. Обычно это связано с «неуловимостью» дольковых раков на маммограммах, едва заметными маммографическими изображениями в одной проекции, редко содержащими микрокальцинаты, в отличие от протоковых раков (Evans, 1997).
Evans и его группа исследовали ценность обнаружения DCIS в маммографическом скрининге и показала, что обнаружение на маммограммах кальцификации высокого риска позволят диагностировать оккультные, сосуществующие с DCIS инвазивные РМЖ 3-й степени злокачественности. Сравнение в этих сериях биологических характеристик DCIS, выявленных при скрининге, с неинвазивными протоковыми РМЖ, выявленными при клиническом исследовании, неожиданно показало высокую пропорцию неблагоприятных прогностических характеристик DCIS, обнаруженных в скрининге. Наиболее подходящим объяснением этих находок является радиологическое разнообразие маммографических изображений различных подтипов DCIS. Так, DCIS высокой степени злокачественности проявляет себя явно анормальными маммографическими изображениями в отличие от DCIS низкой степени злокачественности. Гранулоподобные и точечные кальцификаты, наблюдаемые при DCIS низкой степени злокачественности, более неуловимы, менее специфичны для рака, и часто не воспринимаются радиологами на маммографическом скрининге из-за схожести с обычной, часто встречающейся доброкачественной патологией молочной железы (Evans, 1994; Holland, 2004).
Инвазивный РМЖ представляет собой злокачественную опухоль, часть которой или вся прорастает базальную мембрану эпителиальной выстилки протока или дольки. Прогноз зависит от двух групп вариабельностей. Первые из них – время-зависимые вариабельности, определяющие стадию рака: размер опухоли, наличие регионарных или отдаленных метастазов. Вторая группа вариабельностей определяет «внутренние» биологические черты опухоли: гистологический тип, степень злокачественности, экспрессия рецепторов гормонов, факторов роста и другие молекулярные характеристики опухоли. Из перечисленных признаков размер опухоли, гистологический тип, степень злокачественности, инвазия сосудов, состояние регионарных лимфатических узлов имеют прямое отношение к исходу заболевания. И клиницисты и патоморфологи согласились с тем, что и для оценки скрининга и для планирования лечения вначале следует ориентироваться на минимальный набор признаков, отраженных в системе TNM от 0 (in situ) до IV стадии.
Установление размера первичной опухоли особенно важно при проведении скрининга. Термин «минимальный» РМЖ первоначально был предложен для идентификации форм РМЖ, характеризующихся особенно благоприятным прогнозом. Gallager (1971) относил к «минимальным» РМЖ все формы рака in situ (протоковую и дольковую) и инвазивные раки не более 5 мм в диаметре. Впоследствии термин был пересмотрен с учетом задач маммографического скрининга, и, в частности, Американская коллегия хирургов, а затем и радиологи приняли размер в 10 мм и менее как стандарт, определяющий «минимальный» РМЖ. Размер опухоли – важный критерий оценки качества скрининга и определения возможностей рентгеномаммографии выявлять не пальпируемые опухоли. Поэтому чрезвычайно важно, чтобы патоморфологи измеряли диаметр опухоли как можно более точно. Чем меньше размер первичной опухоли, тем больше вероятность ошибки в определении ее размера.
В связи с планированием скрининга возникает главный вопрос о том, могут ли быть излеченными больные РМЖ (Моисеенко В.М., 1997). Как это не покажется странным, концепция излечимости даже операбельных стадий РМЖ остается дискутабельной, так как смертельные исходы у больных РМЖ случаются в любые временные интервалы: короткий (до 5 лет), промежуточный (5-10 лет) и длительный (от 10 до 30 лет). Эксперты ВОЗ и Международного агентства по изучению рака (МАИР – IARC) выделяют три концепции излечения рака: статистическую, клиническую и персональную. Haybittle (1991), исследуя проблему курабельности, пришел к неутешительному заключению, что нет убедительных свидетельств «статистического» или «клинического» излечения РМЖ в серии леченных больных, но четверть этих пациентов имеет опыт «индивидуального» излечения, умирая от других причин без признаков прогрессии РМЖ. Этот взгляд базируется на анализе небольшого числа крупных исследований с длительным периодом наблюдения (до 30 лет). На протяжении всех 30 лет регистрировалась постоянно более низкая выживаемость среди больных РМЖ по сравнению с подобранным по возрасту контролем здоровых женщин (не имеющих РМЖ). Однако, по признанию автора, некоторые случаи «поздней» смерти больных РМЖ скорее следовало бы отнести к осложнениям лечения, а не к прогрессированию заболевания. Уровень «индивидуального» излечения больных РМЖ, получавших лечение в последние годы, представляется более высоким благодаря благоприятному распределению по стадиям с уменьшением удельного веса распространенных опухолей. К тому же показано, что смертельные исходы встречаются редко через 20 лет после установления диагноза (Joensuu, 1995). Автор приходит к выводу о принципиальной возможности излечения РМЖ. Исследование, проведенное в Англии (Blamey, 2000), показало, что продолжительность жизни пациентов, умирающих от РМЖ, не подвержена влиянию время-зависимых характеристик опухоли (размер, статус регионарных лимфатических узлов), влияющих на сам риск смерти, а в большей степени определяется «внутренними», присущими опухолями биологическими факторами, такими как степень злокачественности. Среди женщин, умирающих от РМЖ, 90% смертей случаются в пределах 8 лет от момента установления диагноза РМЖ 3-й степени злокачественности, в пределах 13 лет – у больных с опухолями 2-й степени злокачественности, и сроки отодвигаются до 30 лет (!) у больных с опухолями 1-й степени злокачественности. Кривые выживаемости больных РМЖ 2-3 степеней злокачественности (после того, как произошло 90% смертей в популяции) становятся зеркальным отображением кривых для общей популяции. Больные РМЖ 1-й степени злокачественности вообще характеризуются чрезвычайно низким риском смертности. Эти результаты дали основание экспертам МАИР сделать вывод о том, что не все больные инвазивным РМЖ имеют системное заболевание ко времени установления диагноза (IARC, 2002).
Ключевая концепция скрининга - это обнаружение настолько раннего заболевания, что проводимое далее лечение изменяет его прогноз и дальнейшее «естественное» клиническое течение. Однако РМЖ представляет собой гетерогенное многоликое заболевание, что может существенно повлиять на эффективность скрининга. Модели скрининга РМЖ обычно основаны на том, что большинство выявляемых опухолей представляют собой инвазивные раки в ранней стадии прогрессии.
Чтобы понять модель скрининга, представленную на рис.1, необходимо знать несколько условий. Во-первых, модель допускает существование периода нераспознаваемого заболевания, когда ранние ступени малигнизации уже имеются, происходит деление клональных клеток, дифференциация и пролиферация клеток, но опухоль еще не может быть обнаружена в скрининге. С точки отсчета, когда опухоль может быть обнаружена с помощью скрининга, начинается так называемое «временное пребывание» («sojourn time» по Zelen, 1969) или «выявляемая доклиническая фаза». Время «опережения» (lead time) означает временной отрезок между фактическим обнаружением опухоли при скрининге и клиническим ее выявлением, если бы не было скрининга (Morrison, 1992). «Sojourn time» широко варьирует при различных опухолях, отражая биологическую и патогенетическую гетерогенность РМЖ. Например, оно зависит от гистологической степени злокачественности опухоли. Среднее «время опережения» в уже проведенных программах скрининга равняется 3–4 годам. Чем короче «время опережения», тем меньше оснований надеяться на успех скрининга и сокращение смертности от РМЖ. В дополнение к этим показателям в оценке качества скрининга чрезвычайно важны два параметра: чувствительность (маммографии) и специфичность скринингового теста. Для скрининга здорового населения считается более важным высокая специфичность теста, то есть минимальное число ложноположительных находок, приводящих к неоправданным биопсиям и, иногда, к избыточному хирургическому лечению.
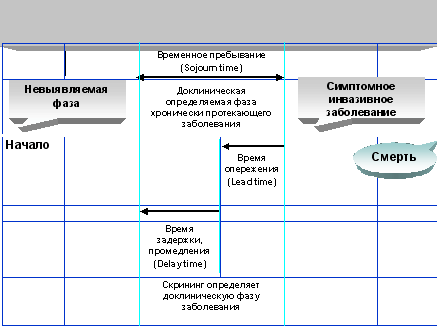
Рис. 1. Схема прогрессии хронического заболевания и скрининг тест для его раннего обнаружения.
Когда популяция женщин подвергается скринингу, далеко не все случаи РМЖ выявляются при первоначальном раунде скрининга, некоторые опухоли диагностируются уже в постскрининговом периоде с помощью клинического метода (пальпации). Это так называемые «интервальные» или межскрининговые РМЖ, обнаруженные у женщин с негативными результатами скрининга. Обычно пропорция интервальных РМЖ колеблется от 15% до 25%. Чем выше частота интервальных (пропущенных при скрининге) РМЖ, тем меньше оснований ожидать снижения смертности в данной популяции. Вероятность выявления рака при скрининге зависит от продолжительности «времени доклинического обнаружения» опухоли (length time detectable preclinically), то есть от «sojourn time». Чем дольше “sojourn time», тем больше шанс обнаружения опухоли. Таким образом, многие опухоли, обнаруженные при скрининге, характеризуются медленным ростом и хорошим прогнозом. Это «отклонение» скрининга получило название «length time bias».
Модель скрининга, представленная на рис.1, описывает лишь операционный процесс скрининга, не касаясь биологии канцерогенного процесса. Современные знания о неопластическом процессе позволяют различать многие ступени и события в канцерогенезе, которые могут начинаться с мутации в специфическом генетическом локусе. Развитие рака - долгий процесс, и не все его ступени являются необратимыми. Возможно, в будущем скрининговые методики и процедуры будут направлены на распознавание этих ранних молекулярно-генетических изменений. Тогда потребуются более сложные модели скрининга.
А пока маммография остается основной составляющей скрининга. Рентгеномаммография как скрининговый тест была всесторонне изучена и оценена в рандомизированных испытаниях, в которых женщины с ранее диагностированным РМЖ были исключены из числа участников. Почти во всех испытаниях (в 7 из 8) было показано, что эффект раннего обнаружения инвазивного рака проявляется через 5–7 лет от начала скрининга. Иными словами, снижение смертности от РМЖ отсрочено даже при хорошо организованном и качественно проведенном скрининге. Позитивный эффект может проявиться и значительно позже, если женщины, участвующие в скрининге, моложе 50 лет (Tabar, 1997), как это наблюдалось в Шведском исследовании. По мере внедрения популяционных программ скрининга (в масштабах страны или региона) методики, разработанные в рандомизированных испытаниях, должны быть адаптированы к более сложной ситуации практического здравоохранения. В противоположность рандомизированным испытаниям, в популяционных программах скрининга потребуется значительно более длительный интервал (более 7 лет) для демонстрации снижения смертности от РМЖ. В отличие от женщин-добровольцев в экспериментальных исследованиях скрининга, общая женская популяция часто колеблется в вопросе участия в предлагаемой программе, а женщин с уже выявленным и ранее леченным РМЖ нелегко исключить при расчетах показателей общей смертности.
Установление точных показателей смертности возможно при наличии канцер-регистра и хорошо отработанной связи с базой данных программы скрининга. Поэтому предсказывающие оценки скрининга, основанные на краткосрочных критериях, являются полезными для определения будущего ожидаемого снижения смертности от РМЖ. К краткосрочным критериям относятся такие параметры как «чувствительность» и «временное пребывание». Оба критерия, в конечном итоге, отражают частоту и удельный вес пост-скрининговых интервальных РМЖ (Das, 1996). Такой прием установления целесообразности скрининга может быть полезным лишь в начальных ступенях программ скрининга, но не в состоянии подменить последующий анализ и установление наблюдаемой (фактической) смертности.
Эффективность использования маммографии в качестве основного теста скрининга проверена в многочисленных рандомизированных испытаниях, проведенных в США (Shapiro, 1966), Шотландии (Alexander, 1999), Канаде (Miller, 1992), Швеции (Tabar, 1999; Andersson, 1997; Nystrom, 2002), Финляндии (Hakama, 1997). Наряду с несомненной пользой маммографии, заключающейся, в конечном итоге, в снижении смертности от РМЖ, имеются и некоторые проблемы. Среди них и упоминавшаяся выше «сверхдиагностика» (over diagnosis), т.е. обнаружение случаев РМЖ, которые никогда бы не были найдены без скрининга на протяжении всей жизни (до 80–90 лет) пациента. Сверхдиагностика увеличивает стоимость скрининга, усложняет оценку программ, но не приносит пользу пациенту, так как выявленное заболевание не угрожает его здоровью. От 5% до 25% выявленных при маммографии опухолей можно отнести к разряду «сверхдиагностики».
В связи с проблемой сверхдиагностики, прежде всего, рассматриваются неинвазивные РМЖ, в частности протоковая карцинома in situ. Ретроспективные исследования показали, что клинически определяемая (пальпируемая) форма DCIS прогрессирует в инвазивный рак в 65% случаев (В.В. Семиглазов, 2001; 2003; Holland, 2004). Как часто переходят в инвазивный рак не пальпируемые DCIS, выявляемые только с помощью маммографии, остается неясным. Результаты испытаний Канадского скрининга показали, что обнаружение и последующее лечение DCIS не привело к сокращению частоты возникновения инвазивного РМЖ на протяжении 11 лет наблюдения. Современные работы свидетельствуют о том, что прогноз DCIS в значительной мере определяется степенью ее злокачественности. Поэтому скрининг может представлять большую пользу женщинам с определенными формами DCIS, например, с опухолями 2-3 степеней злокачественности. Для других форм DCIS остается открытым вопрос, перевешивает ли потенциальная польза их обнаружения при скрининге побочный эффект (тревога, ненужная операция, лучевая терапия).
Среди других проблем, связанных с применением маммографии, обсуждается ее лучевое канцерогенное воздействие на ткань молочной железы. Воздействие радиации – известный фактор риска развития РМЖ. Величина поглощенной дозы радиации на ткань молочной железы на современных маммографах обычно ниже 3 mGy, а доза радиации на щитовидную железу и другие органы вообще незначительная. Риск радиационно-индуцированного РМЖ снижается с возрастом, и особенно низок у постменопаузальных женщин. В модели, основанной на предположении линейной зависимости риска РМЖ от дозы радиации, число смертельных исходов от радиационно-индуцированного РМЖ равнялось 10-50 на 1 млн. регулярно участвующих в скрининге (среди женщин старше 50 лет, прошедших 10–20 скрининговых процедур). Эти цифры можно сравнить с 30–40 тыс. смертельных исходов от РМЖ за этот же временной отрезок среди женщин старше 50 лет на 1 млн. из общей популяции (IARC, 2002). При этом 10–15 тыс. смертей можно было бы избежать с помощью маммографического скрининга. Если скрининг начинается в возрасте 40 лет, число радиационно-индуцированных РМЖ достигает 100-200 на 1 млн. женщин, участвующих в скрининге. В целом можно утверждать, что величина риска по сравнению с пользой скрининга крайне незначительна, если его начинать с 50-летнего возраста. Риск выше при начале скрининга в возрасте 40 лет.
Анализ типа «стоимость-эффективность» различных программ скрининга показал, что стоимость «спасенного года жизни» колеблется от 3 до 8 тыс. евро, если скрининг касается женщин 50-69 лет и повторяется каждые два года.
Качественно проведенный маммографический скрининг, не лишенный упомянутых проблем, приводит в конечном итоге к существенному (до 30%) сокращению смертности от рака молочной железы. Женщины, которые по различным причинам не принимают участия в маммографическом скрининге, должны быть информированы о том, что не существует других методов скрининга (физикальное обследование, самообследование), которые могли бы также эффективно снизить смертность от этого заболевания.
Список литературы:
1. Моисеенко В.М., Семиглазов В.Ф., Тюляндин С.А. Современное лекарственное лечение местно-распространенного и метастатического рака молочной железы.1997. Спб. Гриффон. 254 с.
2. Семиглазов В.Ф., Нургазиев К.Ш., Арзуманов А.С. Опухоли молочной железы (профилактика и лечение).-Алматы.-2001.-344 с.
3. Семиглазов В.В. Лечение рака in situ молочной железы // Мед. акад. журнал.-2003.-N1.-С.14-22.
4. СемиглазоВ.В.В. Рак in situ. Глава в кн. «Опухоли молочной железы (лечение и профилактика). Алматы. 2001.-С.103-125.
5. Holland R, Faverly D. Ductal carcinoma in situ of the breast.-Baltimore.-1997.-233 p.
6. Silverstein M., Lagios M., Groshen. Et al. The influence of margin on local control of ductal carcinoma in situ of the breast. // N.Engl.J.Med.-1999.-Vol.340.-P.1455-1461.
7. IARC handbooks of cancer prevention. WHO. Breast cancer screening. IARC Press.-Lyon.2002.-229 p.
8. Buerger H. Ductal invasive G2 and G3 carcinomas of the breast are the end stages of at least two different lines of genetic evolution. J.Pathol.-Vol.194.-P.165-17 р.
9. Lakhany S. Atypical ductal hyperplasia of the breast: clonal proliferation with loss of heterozygosity on chromosomes 16q and 17p.J.Clin.Pathol.-1995.-Vol.48/-P.611-615.
10. Lampejo O. Evaluation of infiltrating ductal carcinoma with DCIS component: Correlation of the histological type of the in situ component with grade of the infiltrating component. Semin. Diagn.Pathol.-1994.-Vol.-11.-P.215-222.
11. Stratton M. Loss of heterozygosity in DCIS.//J.Pathol.-1995.-Vol.175.-P.195-201.
12. Tabar L. Update of the Swedish two county program of mammographic screening for breast cancer.//RadiolClin.N.Am.-1992.-Vol.-30.-P.187-210.
13. Tabar L. The natural history of breast carcinoma –what have we learned from screening?// Cancer.-1999.-Vol.86.-P.449-462.
14. Tabar L. A new era in the diagnosis of breast cancer.//Surg.Oncol.Clin.-2000.-Vol.9.-P.233-277.
15. Fujii Genetic progression, histological grade, and allelic loss in DCIS of the breast.//Cancer Res.-1996.-Vol.-56.-P.5260-5265.
16. Chuaqui R. Analysis off loss of heterozygosity on chromosome 11q13 in atypical ductal hyperplasia and in situ carcinoma of the breast.//Am.J.Pathol.-1997.-Vol.-150.P.297-303.
17. Lu Y. Comparative genomic hybridization analysis of lobular carcinoma in situ and atypical lobular hyperplasia and potential roles for gains and losses of genetic material in breast neoplasia.// Cancer Res.-1998.-Vol.-58.-P.4721-4727.
18. Hakama M., Holl K. Aggressiveness of the screen-detected breast cancer.//Lancet.-1995.-Vol.-345.-P.221-224.
19. Hakama M. Implementation of screening as a public health policy.//J.Med.Screen.-1999.-Vol.6.-P.209-216.
20. Evans A. The detection of DCIS at mammographic screening enables the diagnosis of small, grade 3 invasive tumours.//Br.J.Cancer.-1997.-Vol.-75.-P.542-544.
21. Evans A. Screen detected DCIS: Overdiagnosis or an obligate precursor of invasive disease?//J.Med.Screen.-2001.-Vol.-8.-P.149-151.
22. Gallager H., Martin G. An orientation to the concept of minimal carcinoma.//Cancer.-1971.-Vol.28.-P.1505-1507.
23. Haybittle J. Curability of breast cancer.//Br.Med.Bull.-1991.-Vol.-47.-P.319-323.
24. Joensuu H., Toikkanen S. Cured of breast cancer?//J.Clin.Oncol.-1995.-Vol.-13.-P.62-69.
25. Blamey R., Elston C., Pinder S., Ellis I. When is a patient cured of breast cancer?//J.Pathol.-2000.-Vol.-190.-P.44.
26. Zelen M/, Feinleib M. On the theory of screening for chronic diseases.//Biometrika.-1969.-Vol.-56.-P.601-614.
27. Morrison A. Screening of chronic disease.// 2nd ed. New York: Oxford University Press.-1992.-P.33-35.
28. Miller A. The Canadian national breast cancer screening study.//J. Natl. Cancer Inst.-2000.-Vol.-92.-P/1490-1499.
29. Nystrom L. Long-term effects of mammography screening. Lancet. - 2002.-Vol.-359. -P.909-919.