МИШЕНИ ЛЕКАРСТВЕННОЙ ТЕРАПИИ БУДУЩЕГО
Тюляндин С.А.
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России
Опыт применения стандартных методов лечения злокачественных опухолей, таких как хирургическое лечение, лучевая терапия или химиотерапия, показал ограниченность их возможностей. С их помощью в настоящее время удается излечивать чуть больше 50% всех больных. Если при ранних стадиях заболевания операция позволяет вылечивать 50% оперированных пациентов, то лечение местно-распространенных и диссеминированных форм опухолей представляется нерешенной задачей. Химиотерапия малоэффективна при таких наиболее часто встречаемых опухолях как рак легкого, толстой кишки, желудка, простаты. Причинами этого могут быть врожденная и приобретенная лекарственная резистентность, плохое попадание препарата в опухоль и его ускоренный выброс из опухолевой клетки. Назрела необходимость определения новых мишеней для создания противоопухолевых препаратов с отличным от существующих механизмом действия. Это становится возможным благодаря развитию фундаментальной науки, сделавшей более понятным процесс возникновения и функционирования опухолевой клетки.
Злокачественная опухоль - болезнь, в основе которой лежит повреждение генетического материала клетки, ведущее к ее бесконтрольной пролиферации и метастазированию и утере способности программируемой клеточной смерти (апоптозу).
В жизни клетка делится, подвергается дифференцировке, двигается, погибает в ответ на сигналы, получаемые из внешней среды. Эти сигналы посредством контакта могут передавать клетки-соседи или клетки матрикса, а также различные внешние регуляторные молекулы, гормоны, факторы роста и.д., связываясь со специфичным трансмембранным рецептором (рис.1). Захват мембранной частью рецептора сигнальной молекулы (очень часто фактора роста) приводит к активации цитплазматической части рецептора, которая чаще всего представлена тирозинкиназой С. Это в свою очередь запускает целую серию реакций, приводящих к активации молекул-передатчиков сигнала с последующей активацией факторов транскрипции. Именно факторы транскрипции активируют гены или группы генов, вызывая их транскрипцию, трансляцию и синтез соответствующих белков.
Все гены опухолевой клетки можно разделить на две части: онкогены, активация которых приводит или способствует пролиферации клетки и метастазированию опухоли; гены-супрессоры, ингибирующие процесс пролиферации, стимулирующие дифференцировку и апоптоз. В геноме опухолевой клетке содержится поврежденная генетическая информация (мутации, неправильный обмен хромосомами генетической информации, в результате которой происходит потеря информации или чрезмерная активация того или иного гена и т.д.). В результате таких повреждения в опухолевых клетках наблюдается активация онкогенов, стимулирующих процесс клеточного деления, образования опухоли и ее метастазов. И наоборот, часто происходит ингибирование или полное выпадение функции генов-супрессоров, которые могли бы воспрепятствовать бесконтрольной клеточной пролиферации. Соответственно, белки, которые кодируются определенными генами будут подразделяться на онко-белки, запускающие процесс, клеточного деления, стимулируя расплавление матрикса и образования новых сосудов(ангиогенез) и белки-супрессоры, которые отвечают за ингибирование клеточного деления, запуск процесса дифференцировки и апоптоза. Эти белки могут быть факторами роста или рецепторами к ним, передатчиками сигналов, факторами транскрипции, ферментами, ответственными за поддержание пространственной структуры ДНК и т.д.
Понимание этой цепочки взаимосвязанных событий, представленной на рисунке 1 в упрощенном виде, уже сегодня позволило определить новые перспективные мишени для будущей противоопухолевой терапии.
Опухолевая клетка характеризуется чрезмерной экспрессией или активностью факторов роста и рецепторов к ним. Например, при раке молочной железы у 25-30% больных наблюдается чрезмерная экспрессия рецептора HER-2 из семейства рецепторов к эпидермальному фактору роста. Было показано, что экспрессия HER-2 является неблагоприятным прогностическим фактором и сочетается с высокой пролиферативной активностью опухоли, потерей гормональных рецепторов, высокой частотой метастазирования. Моноклональные антитела специфично связываются с определенным рецептором и блокируют возможность передачи через него стимулирующего сигнала, что приводит к опухолевой регрессии. В клинике у больных диссеминированным раком молочной железы была доказана эффективность назначения моноклональных антител к HER-2 (Герцептин).
Назначение Герцептина в чистом виде больным с прогрессированием болезни после многократных курсов химиотерапии эффективно у 15% больных и сочетается со значительной средней продолжительностью жизни (13 месяцев). Добавление моноклональных антител к проводимой индукционной химиотерапии антрациклин-содержащими комбинациями у больных метастатическим раком молочной железы достоверно увеличило частоту объективного эффекта (с 36% до 62%) и среднее время до прогрессирования (с 5.5 до 8.6 месяцев) по сравнению с химиотерапией только.
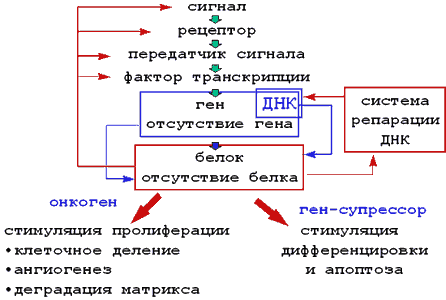
Рисунок 1. Схематическая иллюстрация событий, происходящих в клетке в ответ на получение внешнего cигнала.
Синтезированы химические вещества, способные селективно связываться с рецепторами, блокируя их функцию. Например вещество сурамин блокирует рецепторы тромбоцит-выделяемого фактора роста (PDGF), трансформирующего фактора роста-b (TGF-b), эпидермального фактора роста (EGF) и продемонстрировал противоопухолевый эффект у больных раком простаты и яичников.
Не менее перспективным представляется нарушение функции цитоплазматической части рецептора. Во многих рецепторах факторов роста (рецептор колоние-стимулирующего фактора-1 - CSF-1, EGFR, PDFR, рецептор инсулинового фактора роста-IGFR, рецептор фактора роста фибробластов - FGFR, рецептор фактора роста гепатоцитов - HGFR, рецептор фактора роста эндотелия сосудов VEGFR)) цитоплазматическая часть представлена тирозинкиназой С (ТКС). Фосфолизируясь, это фермент становится активным и в свою очередь фосфолизирует и одновременно активирует молекулы-передатчики сигналов. Синтезирован целый ряд химический соединений, способных ингибировать фосфорилизацию ТКС, тем самым прерывая сигнал, передаваемый мембранной частью рецептора. ZD 1839 и CP 358,774 ингибируют ТКС EGFR и в настоящее время проходят I фазу клинических испытаний. Способностью ингибировать ТКС PDGFR обладают SU101 и CGP 57148, изучающиеся в клинике.
Передатчики сигналов.
Одной из самых изученных молекул-переносчиков сигналов является белок Ras, осуществляющий передачу от тирозинкиназных рецепторов в ядро клетки. Было обнаружено, что ген, кодирующий Ras, содержит мутацию, выявляемую у 90% больных раком поджелудочной железы, 40% раком легкого, 50% раком толстой кишки и 50% раком щитовидной железы. В результате мутации гена Ras белок Ras утрачивает способность терять фосфатную группу и постоянно находится в активированном состоянии, имитируя и передавая стимулирующие к пролиферации сигналы. Таким образом, белок Ras представляется перспективной мишенью для прерывания внутриклеточного сигнала.
Белок Ras для выполнения своей функции должен приобрести соотвествующую пространственную структуру и прикрепиться к врутренней поверхности мембраны. Для этого с помощью фермента фарнезилтрансферазы происходит присоединение 15 фарнезиловых групп на CООН-окончание белка. Без фарнелизации Ras не способен фосфорилироваться и передавать сигналы от рецептора к ядру клетки. Были разработаны ингибиторы фарнезилтрансферазы, которые в экспериментальных моделях показали способность специфично блокировать функцию Ras белка, что приводило к торможению опухолевого роста. В настоящее время эти препараты (L 778,123, SCH 66336, R 115777) проходят I фазу клинических испытаний.
Гены.
Антисенс-терапия.
Антисенс-терапия - это выключение функции конкретного гена за счет ингибирования синтеза кодируемого этим геном протеина. Для этого искусственно синтезируется уникальная последовательность нуклеотидов, которая комплементарно связывается с участком информационной РНК этого гена, тем самым блокируя последующий синтез белка. Последовательность из 15-17 нуклеотидов является единственной во всем человеческом геноме и таким образом обладает абсолютной специфичностью. Уже синтезированы антисенс-олигонуклеотиды, которые блокируют синтез белков, осуществляемый такими онкогенами как bcl-2, c-myb, c-myc, erbB2, Ha-ras, mdm2 и т.д., играющими ключевые функции в канцерогенезе.
Ген с-raf кодирует трионин-специфичную протеинкиназу, которая участвует в передаче пролиферативного сигнала. Была синтезирована последовательность из 34 олигонуклеотидов (ISIS 5132), которая подавляет продукцию белка, кодируемого c-raf. В эксперименте на животных бвло показано, что введение ISIS 5132 обладает минимальной токсичностью, уменьшая продукцию белка с-raf, что существенно замедляет рост опухоли. В настоящее время проводится I фаза клинических испытаний.
У больных неходжкинскими лимфомами низкой степени злокачественности отмечается гиперэкспрессия гена bcl2, который блокирует процесс апоптоза. Благодаря этому опухолевые клетки лимфомы быстро приобретают устойчивость к химиотерапии. В настоящее время синтезирован и проходит клинические испытания олигонуклеотид G3139, состоящий из 18 нуклеотидов и ингибирующий продукцию белка bcl2. Было показано, что препарат обладает минимальной токсичностью: повышение уровня глюкозы в крови и кожная реакция в месте введения препарата. Из 8 больных неходжкинскими лимфомами, резистентными к химиотерапии, у 2 отмечены объективные эффекты. Продолжается II фаза изучения препарата.
Генная терапия.
Как уже было сказано, в основе злокачественного роста лежит повреждение генетического материала клетки. С этих позиций логичным выглядит замена поврежденного гена на нормальный с целью восстановления его функции. Примером подобной генной терапии является восстановление функции гена р53. Ген р53 кодирует белок, который блокирует процесс деления клетки в случае повреждения его генетического материала. В злокачественных опухолях человека часто определяется мутированный ген р53, потерявший способность контролировать процесс клеточной пролиферации. Считается, что мутация гена р53 играет ключевую роль в приобретении клеткой злокачественного фенотипа. Напрашивается простой подход-замена дефектного гена р53 на нормальный, что вновь даст возможность контролировать процесс клеточного деления опухолевой клетки. Нормальный ген р53 получен в достаточных количествах с помощью рекомбинантной технологии. Проблема заключается в том, как осуществить его адресную доставку к опухолевой клетке и включение в геном. Для этого используются вирусы, в частности аденовирус, в геном которого встроен нормальный ген р53. Аденовирус проникает и встраивается в геном опухолевой клетки, доставляя туда и нормальную копию гена р53.
В проведенном исследовании 9 больным немелкоклеточным раком легкого с наличием мутированного гена р53 производили интратуморальное введение аденовируса, содержащего нормальный ген р53. Показано, что перенос нормального гена в опухолевые клетки произошел у всех больных, что привело к заметному увеличению апоптоза. Противоопухолевый эффект был зафиксирован у 3 больных и еще у 3 стабилизация опухоли. Таким образом, заместительная генная терапия демонстрирует значительные возможности даже на первых шагах своего развития.
Ингибиторы циклин-зависимых киназ.
Сегодня понятно, что цикл клеточного деления является сложным многоступенчатым процессом, на разных стадиях которого происходит временная активация регуляторных молекул (циклинов), ведущая к активации определенных ферментов и факторов транскрипции. Для активации различных циклинов на различных фазах клеточного цикла необходимы циклоспецифические циклин-зависимые киназы. Комплекс циклин-циклинзависимой киназы активирует различные белки и факторы транскрипции, необходимые клетке для подготовки к клеточному делению. Ингибирование циклин-зависимых киназ приводит к блокированию клеточного цикла. Два представителя этого класса препаратов проходят клинические испытания.
Флавопиридол, синтетический флавиноид, в экспериментах продемонстрировал арест клеточного деления в момент перехода G1-S и G2-M. Показано, что в основе этого лежит ингибиция циклин-зависимой киназы 1,2 и 4, вероятно за счет потери киназами активных центров фосфорилирования. При проведении I фазы препарат вводился в виде постоянной внутривенной инфузии, и дозо-лимитирующей токсичностью была диарея, контролирующаяся приемом лоперамида. Кроме того, препарат вызывал миалгию, слабость, гриппо-подобный эффект. При суточной дозе 98 мг/м2 в крови была достигнута концентрация флавопиридола, которая в эксперименте была достаточной для ингибирования циклин-зависимых киназ. В настоящее время проводится исследование, в котором инфузия фловопиридола предшествует введению паклитаксела.
Другим препаратом из этой группы является UCN-01, изомер алкалоида стауоспорина, ингибирующий циклин-зависимые киназы 1 и 2. В клинике также испытывается в виде 72-часой постоянной внутривенной инфузии. Дозо-лимитирующей токсичностью являются гипергликемия, тошнота и рвота, легочная недостаточность.
Ингибиторы ангиогенеза.
Сосудообразование (ангиогенез) важнейший компонент опухолевого роста и метастазирования. Опухоль для своего роста нуждается в постоянном образовании сосудов, что обеспечивает достаточное питание и удаление продуктов жизнедеятельности. Опухолевые клетки продуцируют факторы, стимулирующие образование новых сосудов из клеток эндотелия. Инвазия сосудов в опухоль позволяет опухолевым клеткам проникать в кровоток и метастазировать в другие органы и ткани. В настоящее время в клинике изучается около 40 препаратов, ингибирующих различные звенья ангиогенеза. Это моноклональные антитела к рецепторам VEGF и FGF (эти рецепторы передают пролиферативный сигнал клеткам эндотелия), физиологические ингибиторы ангиогенеза (ангиостатин, фрагмент плазминогена, и эндостатин, фрагмент коллагена 18-го типа), препараты, ингибирующие разрушение внеклеточного матрикса, что необходимо для инвазии сосудов (ингибиторы металлопротеиназ, см. далее) и вещества, нарушающие процесс деления эндотелия (TNP-470) или их адгезию к элементам базальной мембраны (моноклональные антитела к интегрину avb3).
Ингибиторы металлопротеиназ.
Важнейшим условием для опухолевой инвазии, ангиогенеза и метастазирования является деградация окружающего внеклеточного матрикса. Опухолевые клетки способны разрушать внеклеточный матрикс за счет продукции семейства трансмембранных протеаз из группы матричных металлопротеиназ. Подавление функции металлопротеиназ в эксперименте приводит не к гибели опухоли, а к ограничению или уменьшению ее размеров, подавлению ангиогенеза и метастазирования. Были синтезированы несколько препаратов, ингибирующих металлопротеиназы, которые находятся на этапе клинического изучения. Проведены I фазы клинических испытаний препаратов маримастат, батимастат, BAY12-9566, AG3340. Учитывая, что ингибиторы металлопротеиназ не обладают прямым цитотоксическим эффектом и при их применении можно ожидать лишь торможение опухолевого роста, в настоящее время проводятся рандомизированные исследования, в которых одним больным назначают химиотерапию, а другим-комбинацию химиотерапии и ингибиторов металлопротеиназ.
Заключение.
За 50-летнюю историю развития химиотерапии FDA дала разрешение на клиническое применение 79 противоопухолевым препаратам. В настоящее время только на различных этапах клинического изучения находятся более 300 новых субстанций, обладающих различными механизмами противоопухолевого эффекта. Это стало возможным благодаря развитию фундаментальных наук, которые позволили понять многие процессы функционирования нормальных и опухолевых клеток на молекулярно-генетическом уровне. Даже если 75% из них будут забракованы по тем или иным причинам, в ближайшие годы можно ожидать удвоения числа лекарственных препаратов, действие которых избирательно направлено на имеющиеся генетические или биохимические изменения конкретной опухолевой клетки конкретной опухоли у конкретного больного. Таким образом, от лечения нозологической формы опухоли мы начинаем переходить к лечению фенотипических и генетических изменений имеющихся в опухолевой клетке. В этой связи возрастает значение молекулярной и биохимической диагностики имеющихся в клетках опухоли отклонений, которая придет на смену постановке морфологического диагноза. Именно характер молекулярно-генетических нарушений в скором времени будет определять выбор лекарственных средств в онкологической клинике и, как хотелось бы надеяться, повысит результативность нашей терапии.
Литература.
1. Bicknell R. New targets for cancer treatment: vessels. Educational book, 23 ESMO Congress, Athens, 1998, p. 61-63.
2. Giavazzi R., Taroboletti G. New targets for cancer treatment: matrix. Educational book, 23 ESMO Congress, Athens, 1998, p. 65-67.
3. GillhamH., Gullick W.J. New targets for cancer treatment: signals. Educational book, 23 ESMO Congress, Athens, 1998, p. 69-84.
4. Kerbel R.S. Some recent advances in preclinical aspects of treating cancer by inhibition of tumor angiogenesis. ASCO Educational book, spring 1999, pp. 4-7.
5. Sausville E.A. Cyclin-dependent kinases: novel targets for cancer treatment. ASCO Educational book, spring 1999, pp. 9-21.
6. Prendergast G.C. Targeting farnesyltransferase: is ras relevant? ASCO Educational book, spring 1999, p.22-28.
7. Shawver L.K. Tyrosine kinase inhibitors: from the emergence of targets to their clinical development. ASCO Educational book, spring 1999, p.29-47.
8. Gallagher W.M., Brown R. P53-oriented cancer therapies: current progress. Ann. Oncol 1999; 10:139-150.
9. Roth J.A. Modification of tumor supressor gene expression in non-small-cell lung cancer with a retroviral vector expressing wildtype (normal) p53. Human Gene Ther 1996; 7:861-74.