Жуков Н.В.
отделение трансплантации костного мозга.
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России
Со времени, когда в 1828 году Томас Ходжкин впервые опубликовал данные о 6 больных с характерным для лимфогранулематоза (лимфома Ходжкина или болезнь Ходжкина) симптомокомплексом [1], в лечении данного заболевания был достигнут значительный прогресс. Благодаря внедрению в клиническую практику эффективных программ терапии I линии, в настоящий момент удается добиться длительной ремиссии у 80-95% больных с ранними стадиями заболевания (I-II стадия) и у 50-70% больных с распространенной болезнью (III-IV стадии) [ 2, 3, 4, 5, 6, 7, 8, 9, 10]. Большинство программ I линии, используемых в настоящее время (CVPP, ABVD, BEACOPP Stanford V и т.д.), успешно освоены онкологами и гематологами стран СНГ, и их применение позволяет добиться результатов, сопоставимых с мировыми. Столь хорошие результаты начальной терапии послужили причиной для того, что бы это заболевание стало рассматриваться многими врачами как одно из прогностически наиболее благоприятных злокачественных новообразований.
Однако у некоторых больных с ранними и у 30-50% пациентов с распространенными стадиями проведение адекватной терапии I линии не позволяет добиться полной ремиссии (первичная химиорезистентность, первично-резистентное течение) или после ее достижения в последующем отмечается рецидив. Эффективность лечения больных первично-резистентной опухолью или с рецидивами после химиотерапии значительно ниже. Разработанные для лечения этих больных многочисленные схемы химиотерапии II линии, включающие цитостатики, не имеющие перекрестной резистентности с препаратами I линии (CEP, CEM, dexa-BEAM, mini-BEAM, DHAP и т.д.), позволяют добиться ремиссии у 30-50% пациентов, однако долговременная безрецидивная/бессобытийная выживаемость не превышает 10-30% [11 , 12, 13, 14, 15, 16].
Данные многих исследований свидетельствуют о том, что повышение доз цитостатиков может преодолеть механизмы резистентности опухолевых клеток. Однако интенсивные режимы II линии, предусматривающие эскалацию доз цитостатиков в 1,3-1,5 раза, при сопоставимой с менее интенсивными режимами эффективности, обычно обладают гораздо большей миелотоксичностью и требуют активной поддерживающей терапии. Интенсивная терапия II линии (DHAP, dexa-BEAM, mini-BEAM и т.д.) может сопровождаться риском смерти от нейтропенической инфекции в 3-5% случаев. Трансплантация клеток предшественников гемопоэза из костного мозга и/или периферической крови позволяет относительно безопасно увеличить дозы цитостатиков 2-10 раз за счет быстрого и эффективного восстановления нормального кроветворения после высокодозной химиотерапии.
Учитывая столь неудовлетворительные отдаленные результаты стандартной терапии II линии, а так же данные о прямой взаимосвязи между дозой цитостатиков и противоопухолевым эффектом, методика высокодозной химиотерапии с трансплантацией аутологичных (собственных) клеток предшественников кроветворения нашла широкое применение при лечении больных с неблагоприятным течением ЛГМ. По данным рандомизированных исследований такой подход позволяет статистически значимо увеличить шанс на долговременную выживаемость у больных с неблагоприятным течением ЛГМ.
В Британском многоцентровом рандомизированном исследовании проведение 1 курса высокодозной химиотерапии по схеме ВЕАМ (кармустин, этопозид, цитозар, алкеран) позволило добиться длительной бессобытийной выживаемости у 53% больных с первично-резистентным течением или рецидивами ЛГМ, в то время как проведение 3-4 курсов интенсивной стандартной терапии II линии по схеме mini-BEAM лишь у 10% больных. Необходимо отметить, что смертность, обусловленная токсичностью проведенного лечения, была сопоставима в обеих группах [17]. Данное исследование даже было прекращено раньше окончания набора планируемого количества пациентов в связи с тем, что больные, информированные о его предварительных результатах, отказывались от включения в группу стандартной терапии II линии.
В Германском многоцентровом рандомизированном исследовании [18] у больных с рецидивами ЛГМ, достигших полной или частичной ремиссии после 2-х курсов интенсивной стандартной химиотерапии II линии dexa-BEAM, проведение высокодозной консолидации ремиссии позволило добиться длительной выживаемости, свободной от неудач лечения (FFTF), в 53% случаев. В контрольной группе, которая вместо высокодозной химиотерапии получала два дополнительных консолидирующих курса dexa-BEAM, этот показатель составил 39% (р=0,025).
Результаты этих рандомизированных исследований дали возможность принять высокодозную химиотерапию в качестве «золотого стандарта» лечения больных с рецидивами лимфогранулематоза в большинстве клиник западной Европы и США. Этому так же способствовало совершенствование поддерживающей терапии, позволившее свести токсическую смертность при ВХТ практически к нулю. Рекомендации проведения ВХТ больным с рецидивами ЛГМ содержатся в наиболее авторитетных руководствах для врачей США и Европы [19, 20, 21 ]. Данные о лечении больных с первично-резистентным течением заболевания более противоречивы, однако в связи с отсутствием эффективного альтернативного лечения, в ряде зарубежных клиник так же придерживаются мнения о необходимости проведения этим больным ВХТ.
По данным регистра европейской организации по трансплантации костного мозга (EBMT) в западной Европе ежегодно выполняется около 1200 -1300 трансплантаций при ЛГМ, что приблизительно соответствует частоте рецидивов и резистентного течения этого заболевания и обеспечивается высокой общей трансплантационной активностью экономически развитых стран (200 – 300 трансплантаций на 10 млн. населения в год).
К сожалению, в странах СНГ данный высоко эффективный метод лечения используется значительно реже. Это отчасти объясняется общим малым количеством трансплантаций (Республика Беларусь – 61, Россия – 11, Украина 0,4 трансплантации на 10 млн. населения), что обусловлено недостаточной технической базой многих клиник. Однако, существуют и субъективные причины сложившейся ситуации, основной из которых является недостаточная информированность врачей гематологов/онкологов и их пациентов о доступности, эффективности и безопасности данного метода лечения в клиниках государств СНГ.
С целью оценки этих показателей нами были проанализированы данные 184 пациентов, получивших ВХТ с трансплантацией аутологичных клеток предшественников гемопоэза из костного мозга и/или периферической крови по поводу неблагоприятного течения лимфогранулематоза в период с января 1990 по март 2003 года. Использовались только данные, полученные из трансплантационных центров, являющихся действительными членами Европейской организации по трансплантации костного мозга (EBMT), отвечающих требованиям по безопасности проводимого лечения и трансплантационной активности данной организации (не менее 20 трансплантаций в год) и изъявивших желание предоставить требуемую информацию. Данные были предоставлены следующими клиниками:
Результаты анализа были доложены и опубликованы в материалах Российско-Норвежской конференции по гематологии в сентябре 2003 года [22].
Медиана возраста больных на момент трансплантации составляла 27 лет (от 11 до 56 лет), было включено 89 мужчин и 95 женщин. Причины принятия решения о проведении ВХТ представлены в таблице 1, характеристика пациентов в таблице 2. В связи с малым количеством пациентов, получивших ВХТ по поводу позднего единичного рецидива (9 больных) при анализе они были объединены с больными, имевшими множественные рецидивы. Под первичной резистентностью понималось отсутствие полной (ПР) или сомнительной полной ремиссии (сПР) после проведения адекватной терапии I линии или прогрессирование заболевания в пределах 3 месяцев после завершения такой терапии. Ранним рецидивом считалось прогрессирование болезни менее чем через 12 но более чем через 3 месяца после достижения ПР или сПР. Больные с прогрессированием в более поздние сроки расценивались как имеющие поздний рецидив. Наличие более одного рецидива расценивалось как множественные рецидивы заболевания.
Таблица 1
Причины проведения ВХТ.
| Первичная резистентность | 44,8% |
| Ранний рецидив | 27,2% |
| Множественные рецидивы/поздний рецидив | 26,6% |
| Первично неблагоприятный прогноз (консолидация I полной ремиссии) | 1,4% |
Таблица 2
Характеристика пациентов на момент принятия решения о ВХТ.
| Стадия | IV | 43% |
| III | 26% | |
| II | 27% | |
| I | 4% | |
| Симптомы интоксикации | 53% | |
| Среднее количество курсов стандартной химиотерапии, проведенных до принятия решения о ВХТ (интервал) | 9 (от 2 до 34) | |
До ВХТ 156 (84,8%) больных получили реиндукцию ремиссии. Под реиндукцией ремиссии понималась стандартная химиотерапия II линии, целенаправленно используемая (входящая в план высокодозного лечения) с целью циторедукции или оценки химиочувствительности опухоли перед ВХТ. В качестве режима реиндукции у 54,5% больных использовался dexa-BEAM (дексаметазон, кармустин, этопозид, цитозар, алкеран), у 16,9% DHAP (дексаметазон, цисплатин, высокие дозы цитозара) и DHAP-подобные режимы, 3,8% другие режимы.
В качестве режима ВХТ большинство (81%) больных получили химиотерапию по схеме ВЕАМ (кармустин, алкеран, этопозид, цитозар), 11% CBV (циклофосфамид, кармустин, этопозид + митоксантрон), 6% больных были проведены другие курсы ВХТ и 2% пациентов получили по 2 курса высокодозной химиотерапии.
В качестве трансплантата костный мозг использовался у 29% больных, периферические стволовые клетки у 54%, комбинированный трансплантат (костный мозг + периферические стволовые клетки) был использован у 17% больных.
ОПРЕДЕЛЕНИЯ И СТАТИСТИЧЕСКИЙ АНАЛИЗ
Под временем принятия решения о ВХТ понималась дата проведения первого курса индукционной (циторедуктивной терапии), или, если таковая не проводилась, дата начала высокодозной химиотерапии.
Общая выживаемость исчислялась от даты начала реиндукции ремиссии (если таковая проводилась), или от момента трансплантации (если реиндукция не проводилась) до даты смерти от любой причины или даты последнего наблюдения.
Безрецидивная выживаемость оценивалась только у больных, достигших после ВХТ полной или сомнительной полной ремиссии. Выживаемость исчислялась от даты трансплантации до даты рецидива или последнего наблюдения за больным (если рецидива не было).
Выживаемость свободная от неудач лечения исчислялась от даты начала реиндукции ремиссии до даты трансплантации (если в результате ВХТ не была достигнута полная или сомнительная полная ремиссия) или до даты смерти от любой причины, или до даты последнего наблюдения (если на этот момент больной был жив в полной ремиссии после ВХТ).
Выживаемость оценивалась по методу Kaplan-Meyer, сравнение выживаемости между группами осуществлялось при помощи log-rank теста.
РЕЗУЛЬТАТЫ АНАЛИЗА
Непосредственная эффективность лечения
После проведения индукционной терапии полной ремиссии достигли 21,2% больных, сомнительной полной ремиссии 3,8 % больных, частичной ремиссии (ЧР) 46,8%, стабилизация болезни (СТ) была отмечена у 12,8%, прогрессирование (ПРГ) у 15,4% больных. После проведения ВХТ полной ремиссии удалось достичь у 57,4% больных, сПР у 10,8 %, ЧР у 15,9%, СТ наблюдалась у 10,8%, прогрессирование у 5,1%.
Отдаленные результаты лечения
На момент анализа медиана наблюдения за живущими пациентами составила 30 месяцев (от 3 до 139 месяцев). При данной медиане наблюдения 5-летняя общая выживаемость составила 60%, безрецидивная выживаемость 69,7%, а выживаемость, свободная от неудач лечения 41,5%
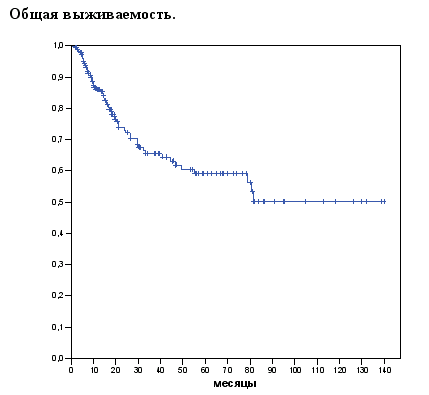
Рисунок 1
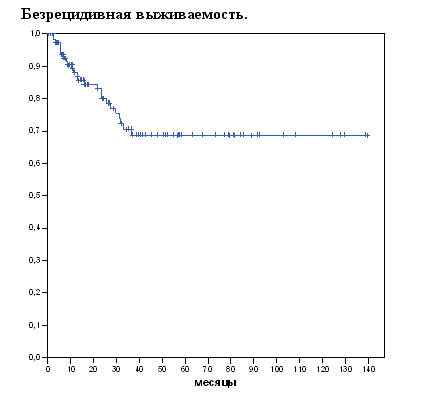
Рисунок 2
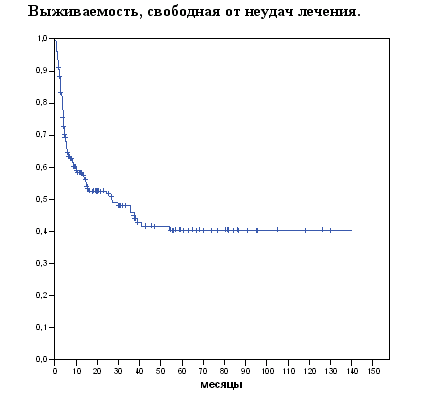
Рисунок 3
Необходимо отметить, что отдаленные результаты лечения в различных центрах статистически значимо не отличались. Как видно из представленных данных в анализируемой группе преобладают пациенты с крайне неблагоприятным прогнозом. Большинство больных, получивших ВХТ, имели первично-резистентное течение болезни (44,8%) или множественные рецидивы (24,6%). Кроме того, даже больные с единичным ранним рецидивом зачастую получали высокодозное лечение лишь при отсутствии эффекта на несколько режимов II линии (резистентный рецидив). В связи с этим был проведен анализ выживаемости в зависимости от типа течения болезни. Общая и безрецидивная выживаемость пациентов, получивших лечение по поводу первичной резистентности, множественных или ранних рецидивов статистически значимо не отличались (р=0,17 и 0,67, соответственно). Лишь при анализе выживаемости, свободной от неудач лечения, была выявлена статистически достоверная разница в зависимости от типа течения болезни (р=0,029).
Выживаемость, свободная от неудач лечения, в зависимости от типа течения заболевания.
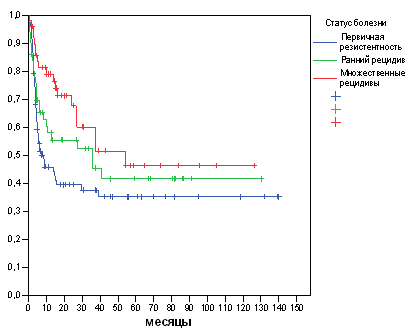
Рисунок 4
Таким образом, несмотря на то, что пациенты с первично-резистентным течением заболевания или множественными рецидивами обычно рассматриваются большинством зарубежных клиник как «малоперспективные» в отношении эффективности ВХТ, данные нашего исследования свидетельствуют о возможности получения длительной ремиссии у 35-45% этих больных. Это, как нам кажется, оправдывает проведение ВХТ у данной категории пациентов, практически не имеющих других шансов на достижение длительной ремиссии. Однако во многом такой контингент больных отражает отношение к ВХТ со стороны онкологов/гематологов стран СНГ. Если в большинстве экономически развитых стран ВХТ в первую очередь проводят больным, имеющим наибольший выигрыш от данного вида лечения (первый рецидив), то в странах СНГ данный метод лечения либо не предлагается больным, либо решение о ВХТ принимается со значительной задержкой.
Нами были отдельно проанализированы результаты лечения больных, получивших ВХТ в соответствии с наиболее распространенными в западных клиниках показаниями: первый ранний чувствительный рецидив (ЧР или ПР после реиндукции ремиссии), отсутствие другой химиотерапии II линии кроме режима реиндукции ремиссии. Таких больных в анализируемой группе было 23, их 5-летняя выживаемость, свободная от неудач лечения составила 59,2%.
В то же время, несмотря на то, что наилучшие результаты ВХТ отмечаются у больных трансплантированных в первом раннем чувствительном рецидиве, вынужденная необходимость проведения ВХТ у пациентов с крайне неблагоприятным прогнозом (первичная резистентность, множественные рецидивы, резистентные рецидивы) позволила накопить опыт лечения больных считающихся в зарубежных клиниках «малоперспективными» и, зачастую, не получающих высокодозного лечения.
Выживаемость, свободная от неудач лечения, у пациентов получивших ВХТ в первом раннем чувствительном рецидиве.
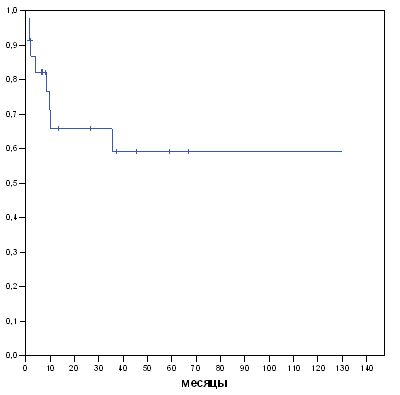
Рисунок 5
Токсичность лечения
К сожалению, еще сохраняется представление о ВХТ, как о крайне токсичной терапии отчаяния, показанной лишь больным, исчерпавшим все возможности стандартной химиотерапии. Как показывает наше исследование, опыт проведения ВХТ, накопленный в активно функционирующих трансплантационных центрах, а так же совершенствование поддерживающей терапии позволяет значительно снизить токсичность ВХТ. Медиана периода времени до восстановления уровня нейтрофилов >0,5*109/л составила 13 дней (от 8 до 90). При использовании в качестве трансплантата только костного мозга эта величина была статистически значимо больше и составила 22 дня, против 13 дней в группе периферических стволовых клеток и 16 дней в группе комбинированного трансплантата. Медиана восстановления уровня тромбоцитов >20*109/л так же составила 13 дней (от 6 до 90 дней), и статистически значимо отличалась в зависимости от вида трансплантата (23, 14 и 18 дней, соответственно). Ранняя посттрансплантационная (100-дневная) летальность составила 5,4% (10 больных). Отмечено уменьшение токсической смертности у более «поздних» пациентов, что, наиболее вероятно, обусловлено увеличением опыта трансплантационных центров, улучшением поддерживающей терапии и т.д. В период с 1990 по 1995 годы токсическая смертность составляла 16%, в период с 1995 по 2000 3,6%, и с 2000 года по настоящее время 1,4% (Рисунок 5).
Ранняя (100-дневняя) летальность больных по годам осуществления ВХТ.
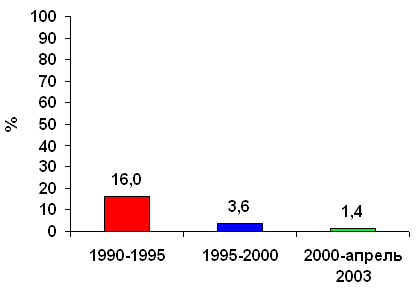
Рисунок 6
ЗАКЛЮЧЕНИЕ
Как видно из анализа данных, более чем 10-летнтий опыт проведения ВХТ в сертифицированных клиниках стран СНГ, позволил добиться эффективности и безопасности лечения, сопоставимой с результатами зарубежных трансплантационных центров. Таким образом, в настоящий момент существуют все предпосылки, позволяющие пересмотреть существующий подход к принятию решения о направлении больного на ВХТ, и привести его в соответствие с мировыми стандартами (проведение ВХТ у больных с первым рецидивом или при резистентности к I линии терапии). Такая тактика позволит сделать высокодозное лечение еще более безопасным, так как множественные курсы стандартной терапии II линии и лучевой терапии, обычно проводимые до ВХТ, приводят к снижению резервов костного мозга и накоплению негематологической токсичности. Кроме того, своевременное проведение ВХТ дает реальный шанс на «разгрузку» онкологических/гематологических стационаров от необходимости госпитализации больных для проведения множественных курсов химиотерапии II линии. Как видно из представленных данных около 40% больных, получивших курс ВХТ, в среднем требующий госпитализации на 20-30 дней, остаются свободными от болезни и, соответственно, не требуют дополнительной терапии более 5 лет.
БИБЛИОГРАФИЯ