Ю.А. Барсуков, С.И. Ткачев, Н.Д. Олтаржевская, М.А. Коровина, С.П. Ярмоненко,
А.А. Вайнсон, А.В. Николаев, О.А. Власов, А.Г. Малихов, Д.В. Кузьмичев,
В.М. Кулушев, В.А. Алиев, В.В. Глебовская
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, ООО «НПО Текстильпрогресс», Москва
Приоритетным направлением улучшения результатов лечения больных раком прямой кишки является разработка и совершенствование различных вариантов комбинированного и комплексного лечения. Среди различных вариантов комбинированного лечения наиболее эффективна методика предоперационной крупнофракционной дистанционной лучевой терапии разовой очаговой дозой 5 Гр в течение 5 дней до СОД 25 Гр на линейных ускорителях электронов энергией фотонов 6-18 МэВ. Эффективность данной программы лечения доказана результатами проспективного рандомизированного исследования, проведенного в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России (протокол №1-03/78, 1978-1984 гг.) (рис. 1).
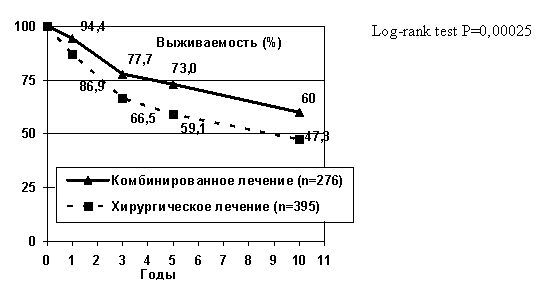
Улучшение отдаленных результатов лечения достигается за счет снижения частоты локорегионарных рецидивов в условиях неоадъювантной лучевой терапии в 2,3 раза без различий в частоте отдаленных метастазов. Так, частота рецидивов при хирургическом лечении составила 19,8%, в то время как при комбинированном – 8,7%. Достоверных различий в частоте отдаленных метастазов не получено (15,2% - при хирургическом лечении и 12,6% - при комбинированном).
В то же время, несмотря на то, что при комбинированном лечении частота рецидивов рака уменьшается в 2,3 раза, все же у 8,7% пациентов в различные сроки диагностируются локорегионарные рецидивы рака. В механизме возникновения локорегионарных рецидивов рака одним из важнейших и определяющих моментов является недостаточное канцероцидное воздействие, в первую очередь на радиорезистентные гипоксические клетки опухоли, доз облучения, используемых при неоадъювантной лучевой терапии. Это обосновывает поиск таких программ комбинированного лечения, при которых усиление неоадъювантного лучевого повреждения злокачественных новообразований достигалось бы не за счет простого наращивания суммарной дозы излучения, что чревато ростом послеоперационных осложнений, а основывалось бы на преодолении радиорезистентности гипоксической фракции опухолевых клеток. Наиболее перспективным в этом плане является использование в клинической практике различных радиомодификаторов, особенно разнонаправленного действия. Наибольший опыт накоплен по использованию локальной СВЧ-гипертермии, являющейся мощным радиосенсибилизатором гипоксических опухолевых клеток в процессе лучевой терапии.
Опыт ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России по применению локальной СВЧ-гипертермии у 230 больных свидетельствует о снижении частоты рецидивов рака и улучшении отдаленных результатов лечения по сравнению с предоперационной лучевой терапией в самостоятельном варианте и хирургическим методом лечения (протокол рандомизированного исследования №1-03/84 1984-1990 гг.). Локальная внутриполостная СВЧ-гипертермия (ГТ) осуществлялась с частотой электромагнитных колебаний 60 МГц в течение 60 мин. при температуре 43,5-44,0оС. Полученные результаты комбинированного лечения с использованием предоперационного термолучевого компонента у больных с промежностной локализацией опухоли (нижне- и среднеампулярные раки) свидетельствуют о достоверном снижении частоты локорегионарных рецидивов до 4,7% по сравнению с хирургической группой (20%) и использованием только предоперационной лучевой терапии (ЛТ) (11,1%) .Это приводит к достоверному улучшению отдаленных результатов лечения, особенно при использовании термолучевого компонента комбинированного лечения (рис. 2).
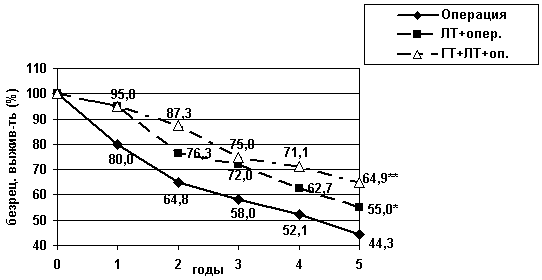
Рис. 2. Безрецидивная выживаемость больных раком дистальных (нижне- и среднеампулярного) отделов прямой кишки в зависимости от метода лечения.
Таким образом, полученные данные свидетельствуют об усилении повреждающего действия лучевой терапии на опухоль при использовании локальной внутриполостной СВЧ-гипертермии. Это подтверждается и показателями лучевого патоморфоза при использовании двух методик комбинированного лечения. Так, при сочетанном использовании лучевой терапии и локальной внутриполостной СВЧ-гипертермии III степень лучевого патоморфоза диагностирована у 21,3% пациентов, в то время как при лучевой терапии в монорежиме - лишь у 9,2%. Это позволяет утверждать, что дальнейшие перспективы повышения эффективности лучевого или термолучевого компонента комбинированного метода лечения лежат в диапазоне одновременного или последовательного использования нескольких радиомодификаторов, желательно разнонаправленного действия, т.е. необходимо стремиться к реализации концепции полирадиомодификации в программе комбинированного или комплексного лечения рака прямой кишки. Таким образом, в современном понимании полирадиомодификация - это одновременное или последовательное применение двух или нескольких разнонаправленных радиомодулирующих агентов в процессе лучевой терапии (С.П. Ярмоненко, 1982).
Такими радиомодифицирующими агентами, помимо СВЧ-гипертермии, могут быть электронно-акцепторные соединения, в частности метронидазол (МЗ) и его производные (С.П. Ярмоненко, А.А. Вайнсон, 2004), а также некоторые химиотерапевтические препараты, такие как 5-фторурацил, являющийся синхронизатором опухолевого цикла, цисплатин, представляющий собой ингибитор сублетальных и потенциально летальных опухолевых повреждений (А.В. Бойко с соавт., 2005). О применении в процессе лучевой терапии нескольких радиомодификаторов, таких как локальная СВЧ-гипертермия и гипергликемия при неоперабельном раке прямой кишки сообщает Б.А. Бердов с соавт. (1996 г.), а использованию метронидазола и локальной СВЧ-гипертермии посвящено исследование А.И. Кожушкова (1989 г.). Такие программы применяются в основном при лучевой терапии неоперабельных местно-распространенных злокачественных опухолей, являющихся радиорезистентными.
Полирадиомодификация с использованием двух радиомодификаторов. В основу создания программы полирадиомодификации с использованием двух радиомодификаторов – локальной СВЧ гипертермии и метронидазола - положены данные о синергизме процессов радиосенсибилизации и гибели гипоксических опухолевых клеток при совместном их применении. Как было сказано выше, эффективность локальной СВЧ-гипертермии в комбинированном лечении рака прямой кишки доказана результатами проспективного рандомизированного исследования, проведенного в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России. Для введения в программу полирадиомодификации второго радиомодификатора, а именно электронно-акцепторного соединения метронидазола, необходимо было разработать технологию изготовления радиосенсибилизирующей смеси, содержащей метронидазол, для внутриректального применения. Необходимыми условиями при создании радиосенсибилизирующей смеси были следующие требования:
На основании опыта аппликационного использования метронидазола с применением салфеток "Колетекс" сотрудниками ООО «НПО Текстильпрогресс ИА» (Н.Д. Олтаржевская с соавт.) разработана технология изготовления радиосенсибилизирующей смеси с использованием метронидазола в виде новой лечебной формы - гидрогеля на основе биополимера альгината натрия с вязкостью 2,63 Па с добавлением 2% раствора универсального транспортера ДМСО. В состав радиосенсибилизирующей смеси входили:
Для определения необходимой концентрации метронидазола в радиосенсибилизирующей смеси было проведено фармакокинетическое изучение его содержания в опухоли при различных (6, 8 и 10 г/м²) концентрациях в радиосенсибилизирующей смеси. Полученные данные (рис. 4) позволили установить, что необходимая для обеспечения радиосенсибилизирующего эффекта концентрация метронидазола в опухоли (180-220 мкг/кг веса) достигается через 3 ч после введения смеси в прямую кишку и требует содержания препарата в радиосенсибилизирующей смеси из расчета 10 г/м² поверхности тела; необходимая концентрация сохраняется в течение последующих 3 часов.
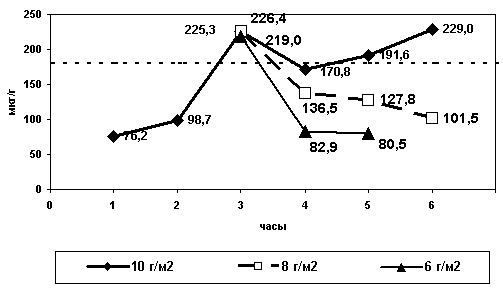
Была использована двукратная внутриректальная аппликация радиосенсибилизирующей смеси. Схема использования полирадиомодификации в схеме комбинированного лечения с применением двух радиомодулирующих агентов представлена на рис. 5.
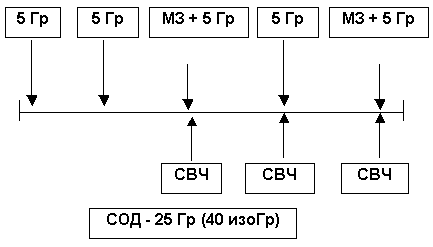
Для профилактики токсического, в т.ч. нейротоксического воздействия метронидазола разработана программа сопроводительной терапии, которая позволила у 92% больных полностью купировать токсические проявления и завершить намеченный курс лечения. Сопроводительная терапия включала следующие мероприятия:
Полирадиомодификация с использованием трех радиомодификаторов. В последние годы выяснилось, что электронно-акцепторные соединения (метронидазол и его аналоги) усиливают эффект многих химиотерапевтических препаратов (эффект хемосенсибилизации). В связи с этим в настоящее время эти соединения рассматривают как перспективные агенты, применение которых позволит без больших затрат повысить эффективность лучевой и химиотерапии при лечении онкологических больных с резистентными формами новообразований.
Повышение эффективности химиотерапии с использованием метронидазола в первую очередь зависит от типа опухоли, времени контакта с клетками, интервала между введением препаратов (И.И. Пелевина с соавт., 1984). Причем для хемосенсибилизации в отличие от радиосенсибилизации, по-видимому, основную роль играет длительное воздействие электронно-акцепторных соединений на клетки перед введением химиотерапевтического препарата (И.И. Пелевина с соавт., 1984). Таким препаратом может быть используемый для лечения солидных опухолей желудочно-кишечного тракта 5-фторурацил. Однако, как показали экспериментальные исследования, комбинация 5-фторурацила и метронидазола оказалась высоко токсичной, и в эксперименте при полном рассасывании опухолей погибали все животные (И.И. Пелевина с соавт., 1984). Уменьшить негативные проявления 5-фторурацила удалось с появлением капецитабина (К), который под влиянием фермента тимидилфосфорилазы превращается в 5-фторурацил непосредственно в опухоли, что уменьшает его концентрацию в плазме крови.
Суточная доза капецитабина в качестве радиосенсибилизатора в сочетании с лучевой терапией и метронидазолом составляет 1500 мг/м² в два приема; препарат принимается внутрь после еды в дни облучения. Методика проведения полирадиомодификации в программе комбинированного лечения рака прямой кишки представлена на рис. 6.
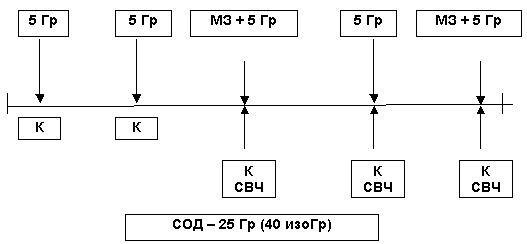
Эффективность разработанных программ полирадиомодификации в комбинированном или комплексном лечении рака прямой кишки изучается в проспективном рандомизированном исследовании. В настоящее время в программу комбинированного и комплексного лечения с использованием полирадиомодификации включены 72 больных. При 2-летнем сроке наблюдения за больными этой группы не выявлено ни одного рецидива. Исследование продолжается.