А.Г. Кедрова
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
Рак яичников (РЯ) в 65-70% диагностируется в стадии диссеминированной болезни. Хотя клиническая ремиссия достигается у большинства больных после комбинированного лечения, прогрессирование заболевания возникает у 80% пациенток. Единой стратегии для наблюдения и лечения больных с устойчивым РЯ на сегодняшний момент нет. Нами рассмотрены цели и задачи лечения персистирующего РЯ, включая классификацию, методы диагностики и терапевтические варианты стратегии. Одна из трудностей в интерпретации результатов второй линии терапии РЯ - гетерогенность группы больных, что приводит к большим погрешностям в подведении результатов. Так, например, чувствительность к карбоплатину при второй линии химиотерапии варьирует от 10% до 40-45% [1]. Точность определений позволит правильно трактовать результаты клинических исследований.
Рецидивный РЯ (потенциально чувствительный к производным платины) встречается у 50% больных и характеризуется возвратом заболевания после достижения полной ремиссии и при ее сохранении длительное время.
В 1994 г. Международная Онкогинекологическая группа (GOG) внесла коррективы: рецидив РЯ, возникший в сроки до 6 мес. после окончания лечения называется “ранний рецидив РЯ” или “платино-резистентный рецидив РЯ”, позднее 6 мес. – “платино-чувствительный” рецидив РЯ [2].
Персистирующий РЯ встречается у 25-30% больных, у которых обнаружена микроскопическая остаточная болезнь после стандартного комбинированного лечения. Например, обнаружена мелкая диссеминация по брюшине при операции “second look” или лапароскопии. В эту же группу входят пациентки с повышенным уровнем СА-125 после окончания лечения при отсутствии объективных проявлений заболевания. Эта опухоль первоначально отвечала на химиотерапию. Она характеризуется медленным ростом, постепенным нарастанием симптомов заболевания, короткими промежутками без лечения, частой сменой лекарственных препаратов второй и последующих линий, частичным ответом на продолженное лечение. Продолжительность жизни таких пациенток иногда превышает 5 и более лет, хотя именно эта группа больных наиболее гетерогенна в связи большой вариабельностью лечения во второй и последующих линиях терапии. При I и II стадиях заболевания персистирующая форма РЯ встречается редко. GOG представляет в отчете только 5,2% (5 из 95).
Рефрактерный рак яичников включает 20-25% больных со стабилизацией или прогрессированием заболевания на первой линии лечения. Это устойчивый к химиотерапии вариант заболевания, имеет самый неблагоприятный прогноз по ответу на вторую линию химиотерапии и продолжительности жизни.
Во многих исследованиях больных со стойким вариантом течения болезни (“ранний рецидив РЯ”, “персистирующий РЯ” и “рефрактерный РЯ”) объединяют в группу “платино-резистентных” больных, хотя чувствительность опухоли ко второй линии терапии у них отличается. Даже в пределах этих, наиболее химиоустойчивых вариантов болезни, разница в эффективности второй линии химиотерапии может достигать 25-30%, а вот медиана продолжительности жизни достоверно не отличается, что говорит о наличии многих других факторов, влияющих на течение заболевания. Механизм развития лекарственной поливалентной резистентности при РЯ еще изучается. Так, уже показано, что высокий уровень экспрессии VEGF-A и COX -2 в опухоли приводит к платиновой устойчивости [3].
Центр нашей дискуссии сегодня – это решение вопроса о необходимости и целесообразности продолженного лечения персистирующего РЯ, а при необходимости терапии - определение точного времени ее начала, выбор метода и продолжительности лечения. Необходимо отметить, что часть таких больных может извлечь пользу не только от системной химиотерапии, но и от внутрибрюшинной, а также от повторной хирургии и лучевой терапии. Из-за множественной диссеминации и нестандартной локализации опухоли при персистирующем РЯ обычные неинвазивные методы диагностики зачастую не позволяют адекватно оценить степень распространенности болезни, что заставляет многих онкологов прибегать к операции “second look” или диагностической лапароскопии после окончания стандартной комбинированной терапии. Ценность и информативность каждого метода диагностики при наблюдении за больными РЯ оценена во многих исследованиях. Так, например, Юго-западная Онкогинекологическая группа сообщила о результатах анализа нескольких исследований по прогностической значимости уровня маркера СА-125 после окончания стандартной терапии РЯ у больных с клинической ремиссией заболевания. При уровне СА-125, не превышающем 10 МЕ/мл, медиана безрецидивного периода составляла 24 мес., при значениях от 10 до 20 МЕ/мл – 17 мес., а при уровне от 20 до 35 МЕ/мл – 7 мес. (p<0,001). Значение маркера не определяло дальнейшую стратегию по поддерживающей терапии, хотя было отмечено, что в группе больных, получавших консолидирующее лечение, маркер продолжал снижаться [4, 5, 6].
Современный стандарт клинической трактовки маркера сводится к следующему: если после комбинированного лечения уровень СА-125 ниже дискретного, а в процессе последующего наблюдения повышается, то необходимо углубленное обследование для выявления локализации и распространенности заболевания. Рекомендации GOG, сформулированные в 2001 г., рекомендуют проводить лечение больных РЯ даже при бессимптомном стойком повышении уровня СА-125 выше 100 МЕ/мл [7]. УЗКТ органов брюшной полости, малого таза, забрюшинного пространства имеет свои ограничения по разрешающей способности. Его информативность при размерах опухолевой диссеминации до 0,5 см составляет всего 30% [8]. Поэтому при стойком повышении уровня СА-125 (при двойном исследовании с интервалом 2 недели) больным необходимо выполнять диагностическую лапароскопию, позитроно–эмиссионную томографию (ПЭТ) или операцию “second look” (рис. 1).
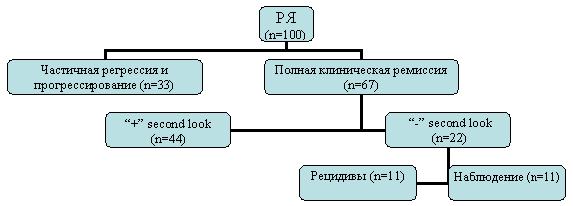
Этой тактики придерживаются многие исследователи, в частности Rubin S. с соавторами показал, что в стандартной группе из 100 больных РЯ III–IV стадий полная клиническая ремиссия зафиксирована у 67 больных, из них морфологически подтверждена только у 22 (22%) [9].
Сравнительный анализ чувствительности и прогностической ценности ПЭТ проведен для выявления персистирующего РЯ в группе больных после окончания комбинированного лечения перед операцией “second look”. Общая чувствительность ПЭТ составила 78%, специфичность - 75%, точность метода – 77%. Степень точности при размерах опухоли более 1 см составила 90% [10]. Ценность диагностической лапароскопии в аналогичной группе больных РЯ составила 90–92% [11, 12]. 8-летнее рандомизированное исследование, изучающее роль лимфаденэктомии при “second look” лапаротомии у больных РЯ II-IV стадиями с полной клинической ремиссией, включило 303 пациентки. Было показано, что безрецидивная и общая 5-летняя выживаемости при полной тазовой и парааортальной лимфаденэктомии составили 41% и 65% соответственно, тогда как при селективной лимфаденэктомии - 49% и 61%. Отметим, что эта операция технически может выполняться не у всех больных [13]. Таким образом, наблюдение за динамикой уровня СА-125 у больных РЯ после достижения клинической ремиссии является обязательным стандартом мониторинга. Даже при медленном, но стойком повышении уровня маркера необходимо добиться убедительных данных о наличии опухоли с помощью других клинико-инструментальных исследований, в том числе лапароскопии, операции “second look” или ПЭТ.
У большинства пациенток удается верифицировать опухоль, и тогда стоит вопрос о выборе метода или схемы терапии. При стойком повышении уровня СА-125 и отсутствии других проявлений заболевания вопрос о времени начала терапии не имеет однозначного ответа на сегодняшний день, учитывая, что уровень маркера может повышаться и при воспалительных реакциях мезотелия, не являясь строго специфичным. Кроме того, в зависимости от свойств опухоли иногда проходят месяцы от первого повышения уровня маркера и объективным проявлением заболевания. В связи с этим продолжаются дебаты относительно выбора оптимального времени начала терапии второй линии у больных персистирующим РЯ. Понятие «активный контроль над динамикой маркера» и «раннее начало терапии» привлекательно для многих пациентов и клиницистов. Аргументами против такой тактики лечения персистирующего РЯ служат медленное течение этой формы РЯ, отсутствие клинических признаков заболевания длительное время, а также тот факт, что любая химиотерапия второй линии ухудшит качество жизни пациентки при невысокой эффективности.
Безусловно, вся цитостатическая терапия связана с побочными проявлениями и отрицательно воздействует на качество жизни больной. Кроме того, многие из малых симптомов, связанных с мелкой диссеминацией, типа дискомфорта в брюшной полости могут сохраниться даже при эффективной химиотерапии второй линии. Таким образом, в отсутствии данных рандомизированных исследований, разумно рассмотреть результаты небольших поисковых протоколов по внутрибрюшинному введению лекарств, по лучевой терапии и по альтернативным не цитостатическим препаратам для пациентов с повышенным уровнем СА-125. Однако эти подходы остаются спорной областью, которая заслуживает вдумчивого коллегиального обсуждения между пациентом и бригадой врачей в каждом конкретном случае.
Помимо точной диагностики распространенности персистирующей болезни, эта группа пациенток должна быть разделена по признаку радикальности первичной операции. Так, если у больных РЯ без остаточной опухоли или с микроскопической болезнью после первичной хирургии и 6 курсов химиотерапии остается мелкая диссеминация и повышенный уровень маркера, то эту опухоль можно отнести к разряду платинорезистентной. Таким пациенткам необходимо сменить тактику лечения: вторая линия химиотерапии, возможно внутрибрюшинное введение лекарств или лучевая терапия. Больные же РЯ с большой остаточной опухолью и имеющие хороший ответ на первичную терапию могут продолжить терапию препаратами первой линии, а затем получать поддерживающую терапию не менее 6 месяцев. Альтернативой служит вторая линия химиотерапии с заменой одного из препаратов первой линии или участие в программных исследованиях по изучению новых биологически активных препаратов: новые ингибиторы тубулина, ингибиторы ангиогенеза, ингибиторы матриксных металлопротеаз, ингибиторы сигнальных механизмов, таргентные молекулы, интерлейкины 2, 6, 12 и т.д.
В поддержку активной стратегии в лечении персистирующего РЯ можно привести результаты нескольких больших исследований, доложенных на заседании ASCO в этом году [14]. Исследование GOG 182-ICON5 хотя и не показало преимуществ трехкомпонентных схем в сравнении со стандартной терапией РЯ, но продемонстрировало необходимость увеличения числа лечебных курсов до 8 у больных распространенным РЯ, что было подчеркнуто в двух докладах на заседании: «Стандарты терапии для распространенного рака яичников: глобальные перспективы».
Результаты исследования SWOG 9701/GOG 178 по изучению роли длительной поддерживающей терапии паклитакселом 175 мг/м² (12 против 3 курсов) у больных распространенным РЯ после достижения полной клинической ремиссии показали медиану безрецидивной выживаемости 22 мес. против 14 мес. (p=0,01). Медиана общей выживаемости составила 53 мес. против 46 мес. (p=0,27). В дополнение к этому был отмечен факт дальнейшего снижения уровня СА-125 в сыворотке крови у больных, получающих поддерживающую терапию. Уровень СА-125 ниже 10 МЕ/мл был достигнут у 175 больных, преимущественно получивших 12 курсов дополнительного лечения. Таким образом, поддерживающая терапия паклитакселом 175 мг/м² в течение года продемонстрировала выигрыш по безрецидивной и тенденцию к увеличению общей выживаемости и была рекомендована в качестве стандарта для больных РЯ с неблагоприятным прогнозом после достижения клинической ремиссии заболевания. При этом, учитывая большое число больных с явлениями периферической нейропатии I-II степени для применения в клинике рекомендована доза паклитаксела 135 мг/м² в течение 12 курсов лечения. [15, 16].
Проблема внутрибрюшинной химиотерапии при лечении рака яичников изучается давно. На сегодняшний день проведены уже несколько рандомизированных исследований: SWOG8501/GOG104 (1996), GOG 114/SWOG9227 (2001), GOG 172 (2006). Результаты упомянутых протоколов были проанализированы на заседании ASCO в 2006 г. (табл. 1).
Таблица 1.
Роль внутрибрюшинной химиотерапии у больных распространенным раком яичников.
| Исследование | Лечение | Результаты |
|---|---|---|
| GOG104: SWOG 8501 | 1 группа: цисплатин внутрибрюшинно 100 мг/м²+ циклофосфан 600 мг/м² в/в
2 группа: цисплатин в/в 100 мг/м² + циклофосфан 600 мг/м² в/в |
увеличение безрецидивной выживаемости на 8 мес. при внутрибрюшинном введении цисплатина |
| GOG 114; больные РЯ II-IV стадий | 1 группа: 2 курса в/в карбоплатин AUC 9, затем 6 курсов внутрибрюшинно цисплатин 100 мг/м² и в/в паклитаксел 135 мг/м²
2 группа: 6 курсов цисплатин 75 мг/м² в/в и паклитаксел 135 мг/м² 24 часовая в/в инфузия |
незначительное превосходство по безрецидивной и общей выживаемости в группе с внутрибрюшинным введением цисплатина, но по токсичности и качеству жизни эта группа уступала контрольной |
| EORTS 55875; включены больные с клинической ремиссией после стандартного лечения паклитаксел + карбоплатин | 1 группа: 4 курса цисплатин 75 мг/м² внутриперитонеально
2 группа: наблюдение |
нет разницы ни по безрецидивной, ни по общей выживаемости |
| GOG172 | 1 группа: паклитаксел в/в 135 мг/м² 24 ч в 1-ый день, цисплатин 100 мг/м² внутриперитонеально во 2-ой день и паклитаксел 60 мг/м² внутриперитонеально в 3-ий день
2 группа: паклитаксел 135 мг/м² в/в 24 ч + цисплатин 75 мг/м² в/в |
снижение риска рецидивов на 28%, медиана общей выживаемости для внутриперитонеального введения - 66,9 мес. для внутривенного - 49,5 мес., т.е. преимущество в 16 мес. по общей выживаемости для больных после оптимальной циторедуктивной операции. |
Общеизвестно, что внутрибрюшинная химиотерапия имеет рациональные составляющие: возможность прямого проникновения лекарственных препаратов непосредственно в опухоль, особенно если имеется большая площадь поражения (мелкая диссеминация по брюшине), возможность увеличить дозы препаратов с минимальными побочными проявлениями (паклитаксел внутрибрюшинно может вводиться в дозе 250 мг/м²). Наряду с тем, что клинические исследования показали преимущество внутрибрюшинной химиотерапии по безрецидивной выживаемости, были зафиксированы и отрицательные стороны такого способа введения лекарств: низкое воздействие на забрюшинную опухоль, печень, плевру, лимфатические узлы (поражаются у больных РЯ примерно в 60% случаев), местная проникающая способность препаратов в опухоль ограничивается 2-3 мм (экспериментальные данные); при внутрибрюшинном введении может возникать боль, присоединиться инфекция, часто нарушается функция кишечника за счет образования массивных спаек, что может привести не только к снижению качества жизни больной, но и развитию кишечной непроходимости и перфорации полого органа; такой метод введения зачастую создает сложности при последующих оперативных вмешательствах [17]. Согласно результатам протокола GOG172, внутрибрюшинная химиотерапия показала некоторое преимущество по безрецидивной и общей выживаемости у больных, прооперированных без остаточной опухоли или с остаточной мелкой диссеминацией. Однако, учитывая токсический профиль такого введения необходимо более тщательно подбирать пациенток для внутрибрюшинного введения, исключая больных после больших травматичных операций с наличием микротравм или резекции кишки, а также с выраженным спаечным процессом и с симптомами раздраженного кишечника. Сложность внутрибрюшинного введения препаратов и снижение качества жизни у многих больных после такого лечения не позволяет рекомендовать внутрибрюшинную химиотерапию как стандарт лечения. При этом необходимо помнить, что этот вид химиотерапии имеет преимущества у ограниченного адекватно отобранного контингента больных РЯ с неблагоприятными факторами прогноза после оптимальной и субоптимальной циторедуктивной операции или операции “second look” при наличии микрометастазов. Последующие оперативные вмешательства у этих пациенток практически невозможны [17]. При изучении фармакокинетики и фармакодинамики при внутрибрюшинном введении препаратов в исследовании GOG172 были сделаны выводы о том, оптимальным является использование внутрибрюшинного введения паклитаксела в дозе 60 мг/м² еженедельно и карбоплатина AUC6 1 раз в 21 день; возможно также чередовать введения, применяя паклитаксел в/в 135 мг/м² 24-часовая инфузия, а в 8-ой день - паклитаксел 60 мг/м² 3 часовая инфузия внутрибрюшинно [18].
Новыми перспективными направлениями для внутрибрюшинной химиотерапии у больных с персистирующим РЯ являются консолидирующая терапия, внутрибрюшинная терапия при положительных находках во время операции “second look”, внутрибрюшинная химиотерапия с гипертермией, внутрибрюшинная иммунотерапия и радиоиммунотерапия с моноклональными антителами YTTRIUM-90 HMFG1. Новые препараты для внутрибрюшинной терапии (интерлейкин 6, интерлейкин 12, Onyx 015, Advexin, FLT3-лиганд, Ontak, tgDDC-E1, EDGEN 001) продолжают изучаться [19]. Исследование бевацизумаба у больных персистирующим РЯ показало его эффективность у 36% больных [20, 21]. Комбинация липосомального доксорубицина 40 мг/м² с карбоплатином AUC6 у 67 больных персистирующим и рецидивным РЯ показала общий эффект 56% при частоте гематологических осложнений 23% [22, 23]. Национальный институт по изучению Рака (США) проводит несколько независимых исследований по изучению персистирующего РЯ у больных с минимальной остаточной опухолью после стандартного первичного лечения: лучевая терапия на область живота с еженедельным в/в введением доцетаксела; гемцитабин в комбинации с карбоплатином в качестве второй линии лечения; тамоксифен в сравнении с талидомидом при повышении маркера без других проявлений болезни. [26, 27, 28, 29].
Таким образом, сегодня существует много вариантов лечения больных распространенным РЯ, много препаратов и комбинаций находятся на стадии изучения. Выбор того или иного метода зависит от множества факторов: радикальность первичной операции, степень чувствительности опухоли к химиотерапии, уровень снижения маркера в динамике в сравнении с исходным, длительность безрецидивного периода, локализация и распространенность персистирующей или рецидивной опухоли, функциональное состояния больной и ее отношение к предлагаемому лечению. При этом нет результатов рандомизированных исследований, которые позволили бы рекомендовать тот или иной лечебный подход, однако при назначении второй линии лечения необходимо помнить о побочных проявлениях каждого из методов, что существенно влияет на качество жизни больной.
Список литературы:
1. Markman M, Hoskins W.// Responses to "salvage" chemotherapy in ovarian cancer: a critical need for precise definitions of the treated population. J Clin Oncol 1992;10:513-514
2. Thigpen JT, Blessing JA, Ball H et al. Phase II trial of paclitaxel in patients with progressive ovarian carcinoma after platinum-based chemotherapy: a Gynecologic Oncology Group study. J Clin Oncol 1994;12:1748-1753, GOG.
3. Engels K., P. Moll, P. Harter // VEGF-A and COX-2 expression correlate with platinum resistance in ovarian cancers.//ASCO 2006, abs. 5062.
4. Liu P-Y, Alberts DS, Monk BJ, et al. Relationship between pretreatment CA-125 level and risk of relapse in advanced ovarian cancer patients in a complete clinical response who received "maintenance therapy". Proc Am Soc Clin Oncol. 2005;23:458s. Abstract 5013.
5. Nadal R. M., B. M. Ojeda, V. Artigas // Stratification of the normal range of CA125 after chemotherapy as a predictive factor in carcinoma of the ovary. ASCO 2006, abs. 5059.
6. H. Tanabe, N. Katsumata, K. Matsumoto// CA125 nadir as a prognostic factor in advanced ovarian carcinoma: A retrospective study of 84 patients achieving clinical CR.// ASCO 2006, abs. 5060.
7. Ozols R.// The conference: Controversies in chemotherapy for ovarian cancer// December 2001, New York.
8. Rubin S, Hoskins W, Saigo P et al. Prognostic factors for recurrence following negative second-look laparotomy in ovarian cancer patients treated with platinum-based chemotherapy. Gynecol Oncol 1991;42:137-41.
9. Sironi S., Messa C., Mangili G., // Integrated FDG PET/CT in Patients with Persistent Ovarian Cancer: Correlation with Histologic Findings// J. Radiology, 2005, Fev.
10. Sijmons EA, Heintz AP. Second-look and second surgery: second chance or second best? Semin Surg Oncol 2000; 19:54-61.
11. Кузнецов В.В., Е.Г. Новикова, А.Г. Блюменберг, И.Корнева// Современный подход при повышении уровня маркера СА-125 у больных раком яичников (РЯ) после комбинированного лечения. Материалы VI съезда Онкологов России, Ростов–на-Дону, 2005 г.
12. F. Landoni, A. Maggioni, T. Dell'anna, et.al.// Randomized trial of systematic lymphadenectomy (LY) vs nodal sampling (SA) at second look surgery (SLS) in ovarian cancer patients: Final results. ASCO 2006, Abs.5068.
13. Bookman M.A., G. Scarfone // Материалы ASCO 2006, Abs. 5002, 5003.
14. Markman Md, P. Liu, S. Wilczynski, B. Monk, L. Copeland, D. Alberts. M. D //Survival (S) of ovarian cancer (OC) patients (pts) treated on SWOG9701/GOG178: 12 versus (v) 3 cycles (C) of monthly single-agent paclitaxel (PAC) following attainment of a clinically-defined complete response (CR) to platinum (PLAT)/PAC. Abs.5005 ASCO2006.
15. Liu Р., J. Moon, D. S. Alberts, B. J. Monk, M. Brady, M. Markman // A modified CA-125 progression criterion in ovarian cancer (OC) patients (pts) receiving maintenance treatment following complete clinical response (cCR) to primary therapy. //ASCO 2006, abs.5080.
16. Wenzel L. B., H. Q. Huang, D. K. Armstrong, J. L. Walker, D. Cella// baseline quality of life (QOL) as a predictor of tolerance to intraperitoneal (IP) chemotherapy for advanced epithelial ovarian cancer (EOC): A Gynecologic Oncology Group (GOG) study. ASCO2006, abs. 5007.
17. Krasner C. N., M. V. Seiden, A. F. Fuller, M. Roche// Pharmacokinetic analysis of an all intraperitoneal carboplatin and paclitaxel regimen in ovarian cancer patients demonstrates favorable systemic bioavailability of both agents ASCO 2006, abs. 50085.
18. Andreopoulou E., F. Muggia, M. Safa, et al. // Phase II study of cetuximab in mucinous peritoneal carcinomatosis. Abs. 14020, ASCO 2006.
19. Wright J. D., A. Alvarezsecord, T. M. Numnum// A multi-institutional evaluation of the safety and efficacy of bevacizumab for recurrent, platinum-resistant ovarian cancer. ASCO 2006, abs. 5019.
20. Cannistra S. A., U. Matulonis, R. Penson, et.al.// Bevacizumab in patients with advanced platinum-resistant ovarian cancer. ASCO 2006, abs. 500.
21. Mirza M. R., B. Lund, K. Bertelsen// Pegylated liposomal doxorubicin (PLD) and gemcitabine (GEM) in combination in the salvage treatment of epithelial ovarian cancer (OC)--a Danish Gynaecologic Cancer Group (DGC) study. ASCO 2006, abs. 5094.
22. F. Hilpert, S. Loibl, J. Huober, et.al.// Combination therapy with pegylated liposomal doxorubicin and carboplatin in malignant gynecologic tumors. A prospective multicenter phase II trial of the AGO-OVAR and the AGO Kommission Uterus (AGO-K-Ut). ASCO 2006, abs. 5095.
23. Radiation Therapy to the Abdomen Plus Docetaxel in Treating Patients With Recurrent or Persistent Advanced Ovarian, Peritoneal, or Fallopian Tube Cancer.// National Cancer Institute (NCI) May 2006.
24. Gemcitabine and Carboplatin in Treating Patients With Persistent or Recurrent Ovarian Epithelial Cancer, Primary Peritoneal Cancer, or Fallopian Tube Cancer That Responded to Previous Cisplatin or Carboplatin.// National Cancer Institute (NCI) August 2006.
25. GOG 198: Randomized Study of Tamoxifen vs Thalidomide in Patients with Biochemical-Recurrence-Only-Epithelial Ovarian Cancer, Cancer of the Fallopian Tube, and Primary Peritoneal Carcinoma After First Line CT. // GOG и National Cancer Institute (NCI) 2006.
26. GOG 01460: Phase II Evaluation of Irofulven in the Treatment o Recurrent or Persistent Platinum-Sensitive Ovarian or Primary Peritoneal Cancer.// GOG и National Cancer Institute (NCI) 2006.
27. GOG-0126M Evaluation of Epothilono-B BMS 247550 in treatment of recurrent or persistent platinum and paclitaxel refractory OC&PP // GOG и National Cancer Institute (NCI) 2006.
28. A Phase II Trial of Cetuximab in Patients with Persistent or Recurrent Epithelial Ovarian or Primary Peritoneal Carcinoma// GOG и National Cancer Institute (NCI) 2006.