Л.А. Ашрафян, Н.В. Харченко, Е.В. Степанова, Н.А. Бабаева, С.В. Ивашина, А.А. Саратян
Российский научный центр рентгенорадиологии МЗ и СР РФ
Несмотря на относительно невысокие показатели заболеваемости, рак вульвы остается важной медицинской и социальной проблемой. Медицинской, потому что, несмотря на то, что рак вульвы является визуально доступной формой рака, более 50% пациенток поступают на лечение с распространенными формами заболевания, а общая кумулятивная 5-летняя выживаемость колеблется от 31,7% до 44,3%. Социальной, потому что более 96% пациенток – это больные постменопаузального возраста, значительная часть которых - старше 70 лет, зачастую с серьезной сопутствующей патологией, что делает невозможным использование радикальных методов лечения.
Как ни при какой другой локализации гинекологического рака, рак вульвы тесно ассоциирован с постменопаузой и инволютивно-атрофическими процессами этого периода жизни женщины. В этом одновременно и парадоксальная особенность этого заболевания и, возможно, ключ к разгадке, пониманию истинных механизмов его возникновения.
Нарастание частоты онкологической заболеваемости по мере старения является универсальной закономерностью, что, вероятно, сопряжено с качественными сдвигами в рамках гуморального и клеточного иммунитета, присущими пожилому и преклонному возрасту, а также, видимо, с накоплением генетических поломок (мутаций) по мере старения. Многочисленные качественные нарушения основных физиологических процессов неминуемо должны привести к стойким изменениям целого ряда гомеостатических параметров. Вульва, являясь гормонозависимым наружным половым органом, неминуемо должна рассматриваться как система, в которой экстраполированы не только гормональная, но и инфекционно-биологическая составляющая. В этом смысле в рамках биологического взаимодействия «макроорганизм – микроорганизм» в зоне вульвы возникает множество противоречий (гормональных, химических, физических, биологических), нарушается годами сложившийся паритет интересов, взаимозависимость многочисленных факторов. В целом в масштабе всего организма нарушения, возникающие в различных органах и тканях, приводят к развитию целого ряда хронических заболеваний, формирующих у пожилых людей синдром полиморбидности.
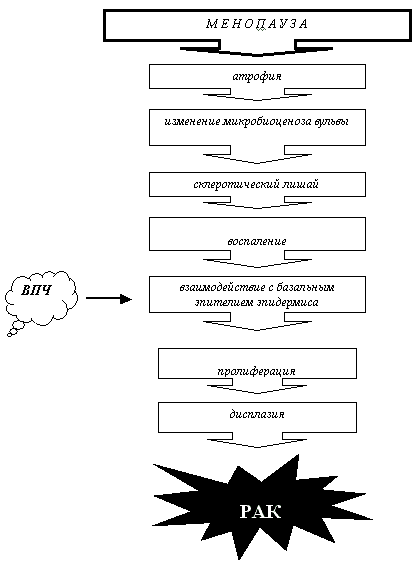
Для вульвы эта закономерность складывается из следующих этапов: возрастная инволюция кожи и слизистой оболочки (на фоне абсолютного дефицита эстрадиола, а также резкого снижения уровня стероидных рецепторов) → развитие инволютивно-атрофических процессов → изменение микробиоценоза вульвы (развитие условно патогенной и патогенной флоры) → формирование воспалительных и дистрофических изменений, травмы и трещины → индуцирование пролиферативных процессов → вклинивание на этом этапе вирусов → развитие дисплазии → прогрессия дисплазии в преинвазивный и инвазивный рак.
В этой последовательности четко прослеживаются два основных аспекта: первый обусловлен эндокринологическими проблемами постменопаузы; второй - микробиологией этой зоны женской половой сферы.
Приступая к формированию этиопатогенетической концепции рака вульвы, мы, прежде всего, опирались на немногочисленные и отрывочные литературные факты, клинический опыт и наблюдения нашего научного центра.
Эндокринологическое направление включало прояснение тех моментов постменопаузального гормонального гомеостаза, которые формируют патогенетическую базу развития тех или иных патологических процессов. Иными словами, почему в одном случае в постменопаузе в органах-мишенях доминируют инволютивно-атрофические процессы, отражающие программу старения, в то время как в других наблюдениях доминируют высоко пролиферативные состояния (дисплазии и рак)?
В рамках формирования нашей концепции особое внимание было уделено двум аспектам: состоянию рецепторного аппарата вульвы и наиболее вероятному источнику продукции метаболитов.
Эндокринология постменопаузы достаточно хорошо изучена. Вместе с тем, в этом разделе гинекологической эндокринологии до последнего времени остается невыясненным вопрос о состоянии рецепторного статуса в органах-мишенях. Изучая уровень эстроген-рецепторов в ткани вульвы, можно отметить, что по мере увеличения продолжительности постменопаузы снижается уровень рецепторов (ЭР+++) в базальном слое с 36% (менопауза <5 лет) до 27% (менопауза 5-15 лет) и 8% (менопауза >15 лет). По прошествии 15 лет постменопаузы в 16% наблюдений имеются ЭР+++ в дерме, в 8% - и в базальном слое и дерме. Таким образом, у трети пациенток постменопаузального периода ткань вульвы сохраняет высокий уровень рецепторов на протяжении длительного времени.
Условия, необходимые для внегонадного стероидогенеза, наиболее интенсивно формируются именно в постменопаузе. С этой точки зрения метаболический синдром является четким и доказанным маркером этих процессов, так как одним из основных проявлений синдрома является ожирение.
Увеличение содержания жира в организме в процессе старения происходит закономерно, даже если и не наблюдается увеличения массы тела. Однако в тех случаях, когда не принимаются специальные меры по ограничению калорийности питания, по мере увеличения возраста наблюдается также абсолютное увеличение массы тела. Здесь уместно заметить, что возрастное ожирение связано не только и не столько с нарушением регуляции аппетита, сколько в существенных нарушениях в энергетическом обмене, которое и создает условие для повышенного накопления жира даже в условиях сбалансированного по калорийности питания. В результате регуляторный тип ожирения дополняется метаболическим типом ожирения. Этот процесс имеет фундаментальное значение не только для механизма формирования ожирения, но и сцепленных с ним болезней. С точки зрения рассматриваемой нами проблемы особую значимость приобретает феномен увеличения биотрансформации андростендиона в эстрон при ожирении. Таким образом, увеличение индекса массы тела в постменопаузе становится фактором риска чрезмерной продукции эстрона, а отсюда и такого метаболита как 16а-гидроксистерон. В наших исследованиях на материале 80 больных раком вульвы средние значения индекса массы тела составили 29,1±4,9 кг/м². При этом у подавляющего большинства больных раком (78,9%) имелось превышение индекса массы тела более 30 кг/м². О значении индекса массы тела для гормонозависимых опухолей (рак эндометрия, рак молочной железы) указано в многочисленных исследованиях. За последние годы появились сообщения и в отношении так называемых гормононезависимых (рак шейки матки) опухолей. Таким образом, формируется убедительная точка зрения в отношении возрастающего онкологического риска у женщин постменопаузального периода в связи с метаболическим синдромом, что еще раз нашло подтверждение на материале наших исследований.
Микробиологическое направление включало изучение широкого спектра (12 видов) инфекционных агентов. Установлен самый разнообразный спектр и ассоциация инфекций не только у больных раком вульвы (82,5%), при склеротическом лишае (74,8%), но также и в контрольной группе (40,7%). Этот факт свидетельствует о глубоких нарушениях в системе микробиоценоза вульвы на фоне постменопаузы. При этом склеротический лишай чаще всего ассоциирован с вирусом папилломы человека (ВПЧ) и гарднереллезом. Плоскоклеточный рак вульвы в 76,2% наблюдений сочетается с ВПЧ. При этом с наибольшей частотой отмечено присутствие 6, 11, 16 и 18 серотипов и реже 55, 59 и 83 серотипов. Кроме того, отмечается абсолютная дупликация 6 и 11 серотипов и полная изолированность 16 серотипа. Причем, для клинически благоприятных вариантов рака вульвы (I-II стадии и ороговевающий рак) характерно присутствие 6/11 серотипов, а также частое сочетание серотипов. При клинически неблагоприятных вариантах рака вульвы (III и IV стадии и низкодифференцированный вариант) доминируют 16 и 18 серотипы ВПЧ; резко возрастает число наблюдений, где ВПЧ не диагностируется, а также абсолютно четко прослеживается феномен отсутствия сочетаний серотипов.
Таким образом, проведенные исследования констатируют ряд важных моментов в эндокринологии и микробиоценозе вульвы. Эти базовые данные как бы формируют основной ответ на вопрос: как на фоне стойких инволютивно-атрофических процессов в зоне наружных половых органов у пациенток постменопаузального периода формируется высоко пролиферативный процесс?
Изменения, происходящие в вульвовагинальной области в постменопаузе, достаточно хорошо изучены и описаны. Темпы развития атрофии урогенитальной зоны в постменопаузе весьма вариабельны и определяются следующими моментами: скоростью развития абсолютной гипоэстрогении и скоростью падения уровня эстроген-рецепторов в базальном слое эпидермиса. Наряду с изменениями поверхностного эпителия редуцируется богатая сосудистая система, многослойный дермальный эпителий вульвы резко истончается и замещается соединительной тканью. Резко возрастает частота микротравм, трещин и мацераций кожи. В связи с истончением эпидермиса создаются реальные условия, когда микротравмы и трещины могут достигать базального слоя. Условно патогенная и патогенная инфекция в этих условиях способна вегетировать на уровне всех слоев эпидермиса, вызывая длительно текущий хронический воспалительный процесс со всеми вытекающими из этого признаками. Атрофия как обязательный и наиболее значимый фактор в этиопатогенезе рака вульвы именно при склеротическом лишае становится наиболее уязвимой и подверженной воздействию вирусной инфекции. Разнообразная и богатая микрофлора, с одной стороны, и выраженная клиническая симптоматика (нестерпимый зуд, расчесы и трещины) с другой, формируют благоприятные условия взаимодействия ВПЧ с базальным эпителием вульвы. Для полной реализации канцерогенного эффекта недостает активной продукции метаболита 16а-гидроксистерона (как это имеет место при раке шейки матки) и его взаимодействия с ВПЧ при участии рецептора.
Становится очевидным, что метаболический синдром и сохраненный рецепторный аппарат в полной мере формируют патогенетическую базу, способствующую эффективному канцерогенезу. В рамках представленной концепции становится ясным, почему не все женщины в постменопаузе заболевают склеротическим лишаем и не у всех больных со склеротическим лишаем развивается злокачественная опухоль.
С учетом этого, склеротический лишай как предрак вульвы может быть обозначен лишь в ситуациях, когда присутствуют три вышеуказанных фактора. И здесь мы сталкиваемся с тем, что понятие предрак приобретает в большей степени биологическое, нежели морфологическое значение. Расширяется граница этого понятия, она сдвигается в сторону его этиопатогенетического осмысления. Иными словами, именно при склеротическом лишае формируются анатомические, микробиологические и клинические условия для интенсивной репродукции ВПЧ. Уже это позволяет считать склеротический лишай неминуемым и обязательным этапом, предшествующим раку вульвы, т.е. – облигатным предраком.
Наконец, последнее. В нашей работе выполнен фрагмент исследования, касающийся уровня белка Е7 в образцах опухоли вульвы при различных серотипах ВПЧ. Положительные данные получены лишь в тех образцах, где имелись 16 и 18 серотипы. Значения онкобелка Е7 были весьма вариабельны и колебались в диапазоне от 0,06 до12 нг/мл. Из 6 больных с вирусонезависимым опухолевым процессом онкобелок Е7 выявлен в одном наблюдении (1,8 нг/мл), что требует отдельного изучения.
Таким образом, обозначены основные факторы, способствующие реализации канцерогенного эффекта на модели рака вульвы у пациенток постменопаузального периода. Учитывая их, можно представить следующую клиническую этапность развития патологических процессов в зоне вульвы.
Наши рассуждения не ставят целью высказать окончательные и сформированные позиции по данной проблеме. Представленные данные могут рассматриваться лишь как информация к размышлению, как факты, призывающие переосмыслить наше понимание проблемы этиологии и патогенеза рака вульвы.