Новости онкологии Прочти об этом раньше, чем твой пациент
15.04.2024
Основным вариантом лечения пациентов с нерезектабельным местнораспространенным немелкоклеточным раком легкого является проведение одновременной химиолучевой терапии с последующей поддерживающей терапией дурвалумабом. В регистрационном исследовании PACIFIC подобный подход обеспечивал улучшение 5-летней общей выживаемости (ОВ) до 42,9% по сравнению с 33,4% в группе ХЛТ + плацебо, а медиана общей выживаемости в группах составила 47,5 и 29,1 мес. соответственно (ОР 0,72; 95% ДИ 0,59-0,89) [1]. В то же время основным показанием для проведения консолидирующей иммунотерапии в данном протоколе являлось отсутствие прогрессирования заболевания на момент завершения ХЛТ, риск которого, по данным разных авторов, приближается к 30% [2-3]. Попытки предупредить подобную диссеминацию или местный рецидив опухоли у трети больных привели к инициации исследования PACIFIC-2, основной задачей которого являлась оценка эффективности и безопасности одновременной химиоиммунолучевой терапии с дурвалумабом [4].
Авторы включили 328 пациентов с нерезектабельным НМРЛ III ст. без предшествующего лечения в анамнезе и рандомизировали их (2:1) в группы одновременной с ХЛТ (экспериментальная группа) или поддерживающей (контрольная группа) терапии дурвалумабом. Согласно представленным в марте 2024 года на ELCC 2024 результатам, авторам не удалось добиться достоверного увеличения выживаемости. Экспериментальная и контрольная группы были хорошо сбалансированы по количеству пациентов с экспрессией PD-L1>1% (51% и 55% соответственно), стадии заболевания (IIIb ст. – 49,8% и 46,8%) и гистологическому варианту НМРЛ (плоскоклеточный рак – 55,3% и 47,7%). При медиане наблюдения в 30,5 мес. медиана выживаемости без прогрессирования (ВБП) составила 13,8 мес. при одновременном проведении химиоиммуннолучевой терапии и 9,4 мес. в группе контроля (ОР 0,85; 95% ДИ 0,65-1,12), однако статистический анализ не подтвердил статистическую достоверность полученных различий (p=0,247) (рис.1).
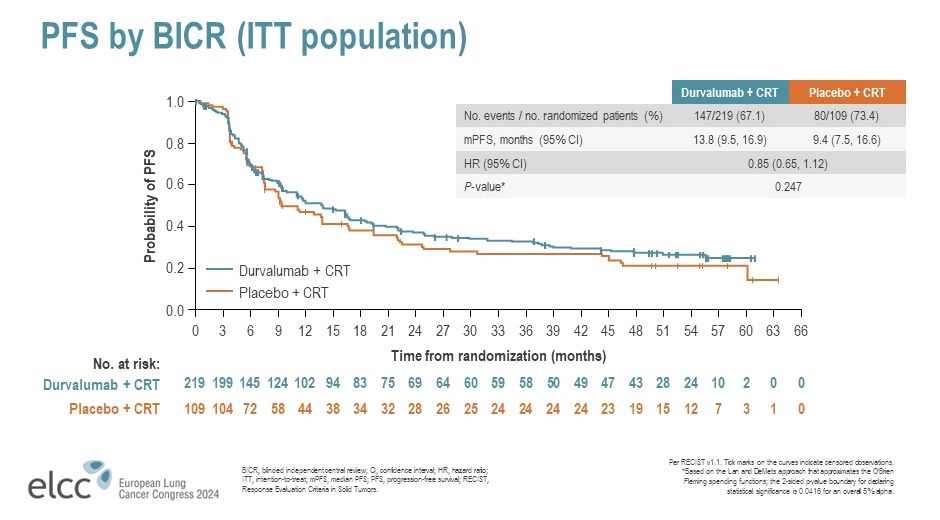
Рисунок 1. Выживаемость без прогрессирования в PACIFIC-2.
Оценка показателя общей выживаемости (ОВ), в свою очередь, не продемонстрировала даже статистически недостоверного улучшения результатов лечения (ОР 1,03; 95% ДИ 0,78-1,39; p=0,823). Частота объективных ответов также была сопоставима между группами – 60,7% (95% ДИ 53,9-67,2%) и 60,6% (95% ДИ 50,7-69,8%). Профиль безопасности лечения в группе одновременной ХЛТ с дурвалумабом по сравнению с последовательным режимом характеризовался большей частотой нежелательных явлений 3-4 ст., развившихся в первые 4 месяца лечения (57,1% против 52,8%), и большим риском развития осложнений, приведших к смерти (6,8% против 4,6%).
Можно заключить, что инициация терапии дурвалумабом на этапе проведения одновременной ХЛТ несколько отдаляет наступление прогрессирования (хоть и статистически недостоверно), но не оказывает никакого влияния на общую выживаемость больных. Более того, прогрессирование на фоне дурвалумаба будет являться противопоказанием для проведения иммунотерапии во II линии лечения, что дополнительно ухудшит онкологический прогноз и, очевидно, сузит диапазон потенциальных лечебных опций для данного пациента. Таким образом, стандартом для неоперабельных пациентов по-прежнему остается проведение одновременной ХЛТ с поддерживающей терапией дурвалумабом, а проблема прогрессирования 30% пациентов на фоне ХЛТ продолжает оставаться открытой.
Источники:
Материал подготовил И.М. Боровков