Новости онкологии Уголок радиотерапевта
10.04.2024
Отношение к лучевой терапии первичного рака почки на протяжении десятилетий имело полярный характер: от широкого применения пролонгированных курсов адъювантного облучения ложа удаленной почки до практически полного отказа от них по причине неэффективности, как было продемонстрировано несколькими анализами. Почечноклеточная карцинома являет собой пример классической радиорезистентности при облучении малыми дозами, однако при этом нам известно множество примеров великолепного эффекта высокодозного облучения метастазов рака почки, в частности, в головном мозге, ведь именно с этого когда-то и начиналась радиохирургия. Лучевой терапии первичных опухолей почки отводилась более чем скромная роль сугубо паллиативного метода: только в случае нерезектабельного рака при наличии болей или макрогематурии. Однако попытки высокодозного облучения, причем не только фотонного, но и протонного, а также нейтронами, предпринимались исследователями во всем мире, и хоть общее число пациентов в этих ретроспективных работах было невелико, результаты порой удивляли.
В январе 2024 года был опубликован систематический обзор Siva et al. [1] по результатам высокодозного облучения методом SBRT/SABR 822 неоперабельных больных почечноклеточным раком из 36 исследований. Медиана частоты локального контроля составила 94,1% (диапазон 70,0-100), 5-летняя выживаемость без прогрессирования – 80,5% (95% ДИ 72-92), а 5-летняя общая выживаемость – 77,2%. (95% ДИ 65-89). Авторы обзора обращают внимание на четыре ключевых клинических вопроса. Во-первых, оптимальное фракционирование дозы составляло 25-26 Гр за одну фракцию или 42-48 Гр за три фракции для более крупных опухолей. Во-вторых, рутинная биопсия после лечения не рекомендуется, поскольку она не позволяет предсказать исход заболевания. В-третьих, SBRT при первичном почечноклеточном раке единственной почки безопасна и эффективна. Наконец, были описаны рекомендации по наблюдению после лечения, которые включают поперечно-осевую визуализацию брюшной полости, включая почки и надпочечники, и обследование грудной клетки каждые 6 месяцев. Этот систематический обзор и практическое руководство поддерживают практику SBRT при первичном почечноклеточном раке как безопасного и эффективного стандартного варианта лечения. Но для дальнейшего продвижения данного опыта и внесения метода в рекомендации, несомненно, необходимы рандомизированные сравнительные исследования с хирургическим вмешательством и инвазивными абляционными методами лечения.
В мартовском номере того же журнала (Lancet Oncology) были опубликованы данные уже проспективного исследования 2 фазы TROG 15.03 FASTRACK II [2], оценившего результаты SABR у первичных больных с верифицированным почечноклеточным раком. Это международное нерандомизированное исследование второй фазы проводилось в семи центрах Австралии и одном центре Нидерландов. Пациенты, имеющие солитарный очаг в почке, были расценены как неоперабельные по медицинским показаниям, имели высокий риск осложнений после операции или отказались от хирургического вмешательства; мультидисциплинарное решение о необходимости активного лечения было обязательным.
Ключевыми критериями исключения были: скорость клубочковой фильтрации менее 30 мл/мин. на 1,73 м2, предыдущая системная терапия почечноклеточного рака, предыдущая высокодозная лучевая терапия в непосредственной близости от очага, опухоли размером более 10 см и прямое контактирование опухоли с кишечником. Пациенты получали либо одну фракцию SABR в дозе 26 Гр для опухолей с максимальным диаметром 4 см и менее, либо 42 Гр за три фракции для опухолей с максимальным диаметром от 4 до 10 см. Первичной конечной точкой был локальный контроль, определяемый как отсутствие прогрессирования первичного почечноклеточного рака. При условии, что локальный контроль в течение 1 года составит 90%, нулевая гипотеза 80% или менее считалась нецелесообразной для перехода к будущему рандомизированному контролируемому исследованию.
В период с 28 июля 2016 г. по 27 февраля 2020 г. было включено 70 пациентов. Средний возраст составил 77 лет (IQR 70-82), 49 (70%) мужчин и 21 (30%) женщина. Средний размер опухоли составил 4,6 см (IQR 3,7-5,5). Все пациенты имели опухоли T1-T2a и N0-N1. Из общего числа 23 пациента получили 1 фракцию SABR в дозе 26 Гр и 47 больных – 42 Гр за три фракции. Медиана периода наблюдения составила 43 месяца (IQR 38-60). Локальный контроль через 12 месяцев от начала лечения составил 100% (р<0,0001), таковым он сохранялся и на протяжении последующего периода наблюдения. Общая выживаемость за 5 лет составила 100% (см. рисунок). У семи (10%) пациентов наблюдались нежелательные явления, связанные с лечением, 3-й степени, наиболее часто – тошнота и рвота (3 [4%] пациента), боль в животе, боку или в области опухоли (4 [6%] больных), толстокишечная непроходимость (2 [3%] больных) и диарея (один пациент, 3%). При этом НЯ 4-й степени не наблюдалось, и смертей, связанных с лечением или опухолевым процессом, также не зарегистрировано.
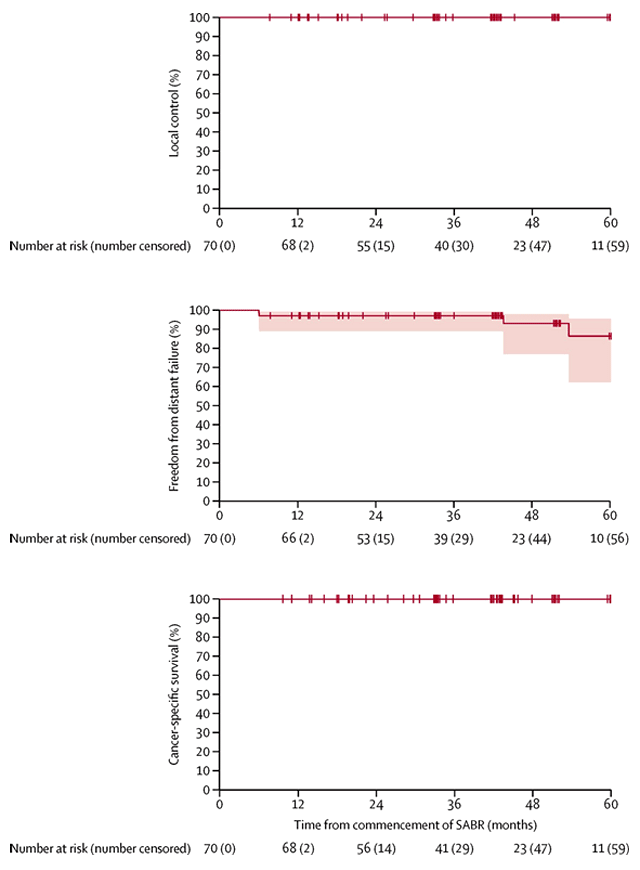
Рисунок. Основные результаты исследования TROG 15.03 FASTRACK II [2].
Насколько нам известно, это первое многоцентровое проспективное клиническое исследование по эффективности радикального нехирургического лечения пациентов с первичным почечноклеточным раком, продемонстрировавшее приемлемый профиль побочных эффектов и удовлетворительную функцию почек после SABR. Вкупе с уже имеющимися ретроспективными данными и систематическими обзорами эти результаты подтверждают необходимость планирования будущих рандомизированных исследований по применению SABR в сравнении с хирургическим вмешательством при первичном почечноклеточном раке.
Источники: